Феноптоз, или Запрограммированная смерть организма
 Мы способны увидеть только то,
Мы способны увидеть только то,
что однажды уже где-то видели.
Ф. Пешоа
История вопроса
Более восемнадцати веков назад римский врач и естествоиспытатель Гален предложил термин «апоптоз», что в переводе с греческого значит «листопад». Так он назвал процесс, обусловливающий опадение листьев осенью. Из хорошо известного факта, что листья опадают только с живых деревьев, сломанные же уходят в зиму с побуревшей, но неопавшей листвой, Гален сделал вывод о «запрограммированности» (говоря современным языком) осеннего отмирания листьев. Очевиден его биологический смысл: зимние снега сломают ветви, если они своевременно не избавятся от листьев.
Сегодня в общих чертах ясен механизм явления, на которое обратил внимание древний ученый. В урочный день и час клетки, формирующие основание черешка листа, совершают акт самоубийства. В результате механическая прочность крепления уменьшается, лист уже не может удержаться а ветке, и его уносит порыв осеннего ветра.
Многочисленные исследования последних двадцати лет убедительно показали, что способность к самоубийству присуща не только клеткам черешка. Скорее это неотъемлемое свойство живых клеток, принадлежащих к самым разным типам, и у растений, и у животных (не исключая и человека). С легкой руки Галена апоптозом стали называть все случаи запрограммированной смерти клеток. Самоликвидируются, например, многие эмбриональные клетки, ставшие ненужными в процессе развития; клетки иммунной системы, вырабатывающие антитела к своим собственным белкам; клетки с поврежденным геномом, а также «бездомные» клетки, случайно оказавшиеся вне родной ткани. Последний случай особенно интересен. Оказалось, что в межклеточной жидкости есть особые белки, специфичные для каждой ткани. Эти белки сорбируются на поверхности клетки и подавляют в них некую систему, генерирующую сигнал самоубийства. Покинув свою ткань, клетка теряет эти белки, запрет исчезает, и в результате клетка кончает с собой. В каком-то смысле клетка многоклеточного организма напоминает глубокого ипохондрика, которого нужно постоянно удерживать от соблазна покончить счеты с жизнью, уговаривать: «Живи дальше!»
Апоптоз - это сложный процесс, жестко регламентированный во времени и пространстве. Его осуществляет большая группа белков, специально созданных в ходе эволюции. При апоптозе клетка разбирает составляющие ее биополимеры (белки, нуклеиновые кислоты и т. д.) на мономеры, которые затем используются другими клетками.
Программы самоликвидации действуют не только на уровне клетки, но также на субклеточном и надклеточных уровнях. Недавно выяснилось, что самоуничтожаться могут митохондрии - внутриклеточные органеллы, ответственные за энергообеспечение. Они окисляют питательные вещества кислородом, а высвобождающуюся при этом энергию превращают в универсальную энергетическую валюту - АТФ. Самоубийство митохондрий я назвал митоптозом по анологии с апоптозом. Митоптоз происходит, например, если митохондрия начинает образовывать из кислорода не воду, а супероксид О2 - предшественник весьма ядовитого гидроксильного радикала ОН-. Появление ОН- запускает программу, ведущую к самоликвидации «впавшей в ересь» митохондрии.
В то же время хорошо известно, что в процессе индивидуального развития некоторые органы возникают, чтобы потом исчезнуть. Недавно выяснилось, как пропадает хвост у головастика, превращающегося в лягушонка: сигналом служит гормон тироксин. Гормон посылает в апоптоз клетки хвоста, а освобождающийся «строительный материал» используется затем для роста и развития лягушонка. Процесс запрограммированного исчезновения органов можно назвать органоптозом.
Итак, запрограммированная смерть органеллы, клетки, органа. А может ли быть запрограммированной смерть всего организма и если да, то как ее назвать? Продолжая аналогию, самоубийство организма можно было бы определить как феноптоз. К случаям феноптоза следовало бы отнести только такие смертельные исходы, причина которых - активация некой заложенной в организм программы. Ниже я попытаюсь убедить читателя в том, что такие программы действительно существуют и парадоксальным образом играют существенную роль в поддержании земной жизни и эволюции.
Закономерный вопрос: каков может быть биологический смысл феноптоза? На первый взгляд смерть особи - ущерб для популяции и вида. Однако это не всегда так, если особь существует не изолированно от сородичей, а является членом сообщества. В этом случае можно представить себе ситуацию, когда альтруистическая смерть индивидуума принесет пользу группе. В принципе феноптоз мог бы служить способом очистки сообщества от индивидуумов, приносящих вред или просто ставших лишними. Вопрос лишь в том, существуют ли врожденные программы самоубийства и действительно ли они включаются, когда особь становится нежелательным членом сообщества.
Самурайский закон биологии
Самоубийство кишечной палочки, не сумевшей исправить поломку в своей ДНК, - это способ обезопасить популяцию от засорения дефектным генетическим материалом. Сложнее объяснить биологический смысл самоубийства пневмококка, отравленного пенициллином. Может быть, здесь речь идет о ликвидации бесплодных членов сообщества (ведь пенициллин останавливает размножение пневмококка). Но вполне возможно, что это просто реакция бактерии на глубокое неблагополучие в ее внутреннем хозяйстве. Даже бактерии, простейшие среди современных живых существ, устроены так сложно, что любой серьезный дефект в их генетике, обмене веществ или поведении, не будучи своевременно устранен, может привести к катастрофическим последствиям для популяции. Для спасения от подобных катастроф природа, по-видимому, изобрела некий механизм, который я назвал «самурайским законом биологии». Вкратце он звучит так: «Лучше умереть, чем ошибиться». А более подробно - «Любая достаточно сложная биологическая система (от автономной органеллы вроде митохондрии и выше) располагает механизмом самоликвидации. Она кончает с собой, если становится потенциально опасной для существования системы, занимающей более высокую ступень в иерархии жизни».
Наглядный пример самоубийства отдельной бактерии во благо сообщества - поведение кишечной палочки, заразившейся некоторыми видами бактериофагов, бактериальных вирусов. В бактериальной клетке фаг безудержно размножается, так что клетка в конце концов превращается в набитый фагами пузырек, который лопается, заражая другие клетки (см. «Химию и жизнь» №3, 2002). Так вот, выяснилось, что кишечная палочка включает механизм самоубийства в ответ на появление некоторых фагов в ее цитоплазме. Причем клетка кончает с собой задолго до того, как в ней накопится большое количество фаговых частиц.
В ответ на появление одного из белков фага бактерия начинает синтезировать собственные белки-убийцы. Описано три типа таких белков, каждый из которых образуется под действием определенного фага. Один из белков формирует отверстие в мембране бактерии, так что все низкомолекулярные вещества вытекают из клетки и она умирает. Другие два белка останавливают систему белкового синтеза: расщепляется либо белок - фактор элонгации Tu, либо лизиновая транспортная РНК. Без этих компонентов невозможен синтез белков - как бактериальных, так и фаговых. В любом из трех случаев самоликвидация зараженной кишечной палочки спасает популяцию бактерий от массового заражения фагом и потому может быть квалифицировано как альтруистическое самоубийство.
Недавно К.-У. Фрелих с сотрудниками описали феноптоз у дрожжей. Массовую гибель их клеток вызывают небольшие количества перекиси водорода, причем этот эффект, как и у зараженной кишечной палочки, требует синтеза каких-то белков. Запрограммированная смерть описана и у простейших - тетрахимен.
Хорошо известна запрограммированная смерть многоклеточных организмов, размножающихся только единожды. У некоторых из них само строение тела несовместимо со сколько-нибудь долгой жизнью. Вспомним поденку: взрослое насекомое этого вида не может есть из-за отсутствия ротового аппарата и погибает вскоре после репродуктивного акта. Другой пример: у клеща Adactylidium потомство прогрызает себе путь на волю из тела матери, вызывая ее гибель.
Однако гораздо чаще при половом акте или тотчас вслед за ним включается поведенческая или биохимическая программа самоубийства. Так, самец одного из видов кальмаров тонет тотчас после спаривания с самкой, которой он подсаживает под кожу свой сперматофор - мешочек со сперматозоидами. Самки некоторых видов пауков при спаривании поедают самцов, с которыми до того мирно сосуществовали. Бамбук живет 10-15 лет, размножаясь вегетативно, а затем зацветает и гибнет, как только созрели семена. Тихоокеанский лосось умирает после нереста, и вовсе не из-за крайнего истощения организма, а вследствие включения особой биохимической программы, в которой ключевую роль играют стероидные гормоны. Если затормозить образование этих гормонов в надпочечниках лосося, он не умрет.
Роль феноптоза не так бросается в глаза у многократно размножающихся организмов. Мы находимся еще в самом начале пути, и не исключено, что он приведет нас к пониманию истинного положения вещей. Тем не менее попытаемся уже сейчас рассмотреть эту проблему, поскольку она может иметь прямое отношение к важнейшим задачам медицины.
Загадка дифтерийного токсина
Очевидно, что животное, инфицированное опасным патогеном, - столь же нежелательный гость в сообществе себе подобных, как и бактерия, заразившаяся фагом. С «надорганизменной» точки зрения быстрая смерть такого индивидуума могла бы стать последней, жестокой, но радикальной мерой предотвращения эпидемии. Вот почему сообщество организмов, способных к альтруистическому самоубийству, должно получить преимущество в борьбе за существование. Рассмотрим для примера дифтерию.
Возбудителем дифтерии служит особый вид коринебактерии. Болезнь сопровождается интоксикацией организма - его отравляет бактериальный токсин, особый белок. Он состоит из двух частей, или доменов, один из которых (большой) узнается особым белком-рецептором во внешней мембране клеток заболевшего человека или животного. После этого другой (меньший) домен токсина перебрасывается внутрь клетки и отделяется от большего. В клетке он действует как фермент, присоединяющий АДФ-рибозу к остатку вещества, называемого дифтамидом. Дифтамид находится во втором факторе элонгации EF-2 - белке, участвующем в белковом синтезе. Дифтерийный токсин инактивирует фактор элонгации и таким образом останавливает белковый синтез. Ферментативная активность токсина весьма высока: одной его молекулы достаточно, чтобы убить клетку. А при массовой гибели клеток умирает и больной.
Дифтамид, объект действия токсина, есть в клетке только в одном белке, причем в одном экземпляре. Остаток аминокислоты гистидина в составе EF-2 превращают в дифтамид пять специальных ферментов, не участвующих в каких-либо других реакциях обмена веществ.
На первый взгляд дифтерийный токсин - оружие коринебактерии в борьбе с макроорганизмом. Однако вот в чем проблема: у дифтамида не обнаружено других функций, кроме как участвовать в убийстве клетки токсином. Более того, клетки с мутантным EF-2, не способным присоединять АДФ-рибозу, имеют нормальный белковый синтез и вообще отличаются от обычных клеток лишь полной устойчивостью к дифтерийному токсину.
Создается впечатление, что дифтамид - мина замедленного действия, которую каждый из нас носит в себе до тех пор, пока не заразится дифтерией. Парадокс получит объяснение, если предположить, что люди и животные используют в борьбе с эпидемией ту же стратегию, что и кишечная палочка, зараженная бактериофагом: смерть под действием дифтерийного токсина позволяет популяции избавиться от инфицированного индивидуума. Вероятно, коринебактерия все равно бы погубила больного каким-либо иным, не зависящим от токсина способом, но это произошло бы после ее массового размножения в организме, который сделался бы опасным источником болезни. В таком случае уже не кажется удивительным наличие дифтамида в одном из важнейших белков. Можно думать, что популяции, не имевшие дифтамида, просто вымерли от эпидемий.
По-видимому, дифтамидный механизм защищает популяцию не только от дифтерии, но от целой группы опасных инфекций. В частности, токсин А, который выделяет одна из инфекционных псевдомонад, действует аналогично дифтерийному токсину, только связывается с другим рецептором. И уже ясно, что это явление уходит своими эволюционными корнями в глубь веков. Дифтамида нет у эубактерий, но он есть у архебактерий и дрожжей.
Септический шок
|
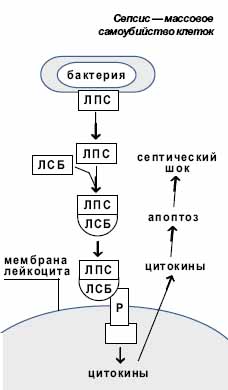
Другой пример патологии, имеющей признаки феноптоза, - септический шок. Многие его черты указывают на то, что смертельный исход специально организован самим организмом, подвергшимся массированному вторжению бактерий. При этом роль бактерий может быть совершенно пассивной. Так называемый эндотоксин, который служит причиной сепсиса, есть не что иное, как липополисахарид, образующий клеточную стенку грам-отрицательных бактерий. Его токсичность всецело зависит от наличия в макроорганизме специальных внеклеточных белков, связывающих его, и белков-рецепторов, узнающих этот белково-липополисахаридный комплекс. Сепсис сопровождается массовым выбросом макрофагами белков-цитокинов, индуцирующих апоптоз (рис. 2). Выключение генов, кодирующих цитокины, ингибирование апоптозных белков или блокирование рецепторов полисахарида снижает токсичность последнего. Можно думать, что путь к победе над сепсисом лежит через описание, а затем блокирование всех путей восприятия и передачи феноптозного сигнала, подаваемого бактериальным липополисахаридом, который сам по себе не опасен. Этот сигнал сообщает о появлении в тканях и крови грам-отрицательных бактерий - потенциально особо опасного класса микроорганизма. Мощная клеточная стенка предохраняет их от воздействия защитных антибактериальных механизмов человека или животного. Не случайно, что именно основной компонент этой стенки играет сигнальную роль. По-видимому, организм реагирует так на любые грам-отрицательные бактерии, в том числе неинфекционные, - они, как известно, также могут вызывать сепсис.
Безусловно, феноптоз служит последней линией обороны сообщества от эпидемии. Когда патогена не слишком много, тот же сигнал - появление липополисахарида - организм использует, чтобы привлечь лейкоциты к зараженному участку ткани. Там лейкоциты образуют цитокины, посылая в апоптоз клетки зараженного участка.
При умеренном уровне инфекции все эти меры призваны спасти, а вовсе не убить организм. Расхожее мнение о сепсисе состоит в том, что он представляет собой чрезмерное использование организмом защитных средств. Но в таком случае неясно, почему эволюция не изобрела контрольного механизма, предотвращающего эту опасность.
Старение организма - особый случай феноптоза?
Мысль о том, что старение как завершающий этап индивидуального развития организма может быть запрограммировано, высказал Август Вейсман в своей знаменитой лекции 1881 года. Вот отрывок из нее: «Я рассматриваю смерть не как первичную необходимость, а как нечто, приобретенное вторично в процессе адаптации. Я полагаю, что жизнь имеет фиксированную продолжительность не потому, что по природе своей не может быть неограниченной, а потому, что неограниченное существование индивидуумов было бы роскошью без какой-либо проистекающей из нее выгоды... Изношенные индивидуумы не только бесполезны для вида, но даже вредны, поскольку они занимают место тех, кто здоров».
В 50-е годы ХХ века гипотеза Вейсмана была раскритикована Питером Медаваром, утверждавшим, что в естественных условиях большинство организмов гибнет раньше, чем успевает состариться, и потому такой механизм не имеет практического значения для вида и не мог быть отобран эволюцией. Однако, по мнению Дж. Боулса (2000), это утверждение неприменимо ко многим видам в определенные периоды их истории. Еще важнее то обстоятельство, что особи с измененным геномом могут сильнейшим образом влиять на судьбу сообщества, даже если они составляют очень малую его часть.
Пример такой ситуации недавно проанализировали У. Мьюэр и Р. Ховард. Они исследовали трансгенный вариант японской аквариумной рыбки, которой ввели человеческий ген гормона роста. В результате рыбки стали расти быстрее. При этом оказалось, что, во-первых, крупные трансгенные самцы более привлекательны для самок и, во-вторых, только две трети трансгенных самцов доживают до репродуктивного возраста. Как показал расчет, взаимодействие этих двух факторов через 40 поколений приведет к полному вымиранию стада из 60 000 рыбок, если изначально в стаде было всего 60 трансгенных особей. За большее число генераций даже одна трансгенная особь может вызвать гибель всего стада.
Подобный прием давно используют для борьбы с вредными насекомыми: подпускают в популяцию некоторое количество стерилизованных самцов. При этом, как и в случае с рыбами, не требуется уничтожать нормальных самцов, которых просто не хватит, чтобы поддержать баланс между размножением и гибелью.
Вероятность какой-либо роковой для популяции ошибки тем выше, чем сложнее устроены организмы. Очевидно, что долгое существование какого-либо вида предполагает совершенство системы защиты геномов индивидуумов, составляющих этот вид. Такая система отвечает за: 1) предотвращение окислительного и любого другого повреждения генома, 2) репарацию поврежденного генома и 3) очистку живых систем от потенциальных монстров с поврежденным геномом. Повреждения накапливаются с возрастом, поэтому смерть от старости могла бы стать способом защиты генома по третьему типу.
Биологическая эволюция оказалась бы невозможной, если б геном оставался неизменным. Но это практически исключено, поскольку любая защита генома не может быть абсолютной. Более того, ухудшение условий среды, как любое отклонение системы от оптимума, должно ослаблять эту защиту и тем самым увеличивать вероятность появления мутаций и новых признаков.
Эта вероятность возрастает также при увеличении плодовитости и ускорении смены поколений - то есть при уменьшении продолжительности жизни. В опытах Д. Резника у гуппи, многие годы живших в среде без хищников, а затем в течение пяти лет - с хищниками, стал раньше наступать репродуктивный возраст, а продолжительность жизни сократилась, даже если убрать хищников.
Итак, долгожительство означает медленную смену поколений и, следовательно, уменьшение шанса возникновения новых признаков при половом размножении. В этом может быть вторая причина запрограммированной смерти старых особей.
Старческий феноптоз мог бы выглядеть как внезапная смерть, наступающая при достижении особью некоего критического возраста. Дж. Боулс упоминает об одном из видов морских птиц, которые внезапно умирают в 50 лет без всяких признаков старения. Однако ясно, что такая ситуация - исключение. Как правило, смерть от старости - результат процесса, сильно растянутого во времени. Но коль скоро речь идет о многократно размножающихся особях, медленный феноптоз может оказаться полезней для вида, чем быстрый. Дело в том, что наличие у особи полезного признака способно в течение какого-то времени компенсировать неблагоприятные эффекты старения, тем самым давая особи репродуктивные преимущества. Крупный, сильный олень даже и в старости имеет шанс оставить потомство, выиграв весеннюю битву за самку у молодого, но низкорослого соперника.
Еще раз о теломерах
По мнению Дж. Боулса, первый специализированный механизм старения был изобретен эволюцией, когда клетка простейшего стала использовать линейную ДНК вместо кольцевой, типичной для подавляющего большинства бактерий. О концевой недорепликации ДНК «Химия и жизнь» писала не раз и не два. Белковый комплекс, копирующий ДНК, был создан эволюцией применительно к кольцевой ДНК и не способен воспроизводить концевые участки линейной матрицы, на что впервые обратил внимание А. М. Оловников. Подобный недостаток присущ и системе репарации ДНК. Почему же эти дефекты в работе важнейших ферментативных систем не были исправлены за миллионы лет эволюции, за то же время разрешившей гораздо более серьезные проблемы? Не потому ли, что сокращение продолжительности жизни на клеточном уровне было чем-то выгодно?
Механизм репликации, по-видимому, был усовершенствован в процессе эволюции таким образом, что к концам кодирующей линейной ДНК были присоединены некодирующие нуклеотидные последовательности, так называемые теломеры. Клетка использовала укорочение теломер для отслеживания числа делений, причем это происходило без повреждений кодирующей части. Таким образом, основная, генетическая, функция ДНК была отделена от новой: мониторинга количества делений.
Укорочение теломер могло бы служить причиной старения таких одноклеточных организмов, как простейшие или дрожжи. У многоклеточных в половых и стволовых клетках постоянно активен фермент теломераза, наращивающий концевые участки. В остальных клетках синтез теломеразы прекращается еще в эмбриональный период развития, так что с возрастом длина теломер только уменьшается, как шагреневая кожа. (Но важно, что прекращение клеточных делений наступает еще до того, как теломера исчезнет вовсе и начнет разрушаться смысловой участок.)
Остается открытым вопрос о том, в какой степени теломерный механизм участвует в старении многоклеточных организмов. Вполне возможно, что они изобрели совсем иные программы старческого феноптоза. Однако несомненно, что у долгожителей уменьшение длины теломер приближается к роковой черте, за которой наступает запрет на деление клетки. По данным группы К. Сасаджимы из Японии, теломеры в клетках печени людей старше 80 лет почти вдвое короче, чем у детей до 8 лет. По-видимому, продлить жизнь тем, кому за сто, можно лишь при условии, что удастся нарастить их теломеры, включив на какое-то время в стареющих тканях теломеразу.
Инфаркт, инсульт, рак: болезнь или закономерность?
Наиболее частые смертельные болезни пожилых людей, а именно инфаркт и инсульт, напоминают феноптоз при септическом шоке в одном важнейшем аспекте. Во всех трех случаях заболевание развивается стремительно и, если не принять экстренные меры, приводит к летальному исходу, причем происходит катастрофическое распространение апоптоза среди клеток, образующих жизненно важные органы.
Вновь возникает недоумение, почему организм допускает такую сильную активацию апоптоза, которая приводит к его гибели. Ответ на этот вопрос можно дать, приняв, что ишемические болезни реализуют программу самоубийства.
Вот почему один из подходов к лечению инфаркта и инсульта - блокирование апоптоза. В нескольких лабораториях уже показано на животных весьма благоприятное действие ингибиторов апоптоза при ишемических болезнях сердца и мозга. К сожалению, применять ингибиторы возможно лишь в острых случаях, то есть сразу после инфаркта или инсульта. Апоптоз необходим для нормального функционирования важнейших систем нашего организма. Более того, он служит одним из рубежей антираковой защиты организма. Поэтому преобладание антиапоптозной системы над апоптозной снизит риск ишемической болезни, но одновременно повысит риск злокачественного перерождения. Известно, что рак, подобно инфаркту или инсульту, есть болезнь преимущественно пожилых. В 50% случаев это обусловлено накоплением мутаций в гене белка р53, «стража генома», активирующего апоптоз. В некоторых других случаях раку сопутствует суперпродукция антиапоптозного белка Bcl-2.
Нельзя не отметить, что человек стареет не так, как его родственники, даже самые ближние. У многих видов животных, включая высших обезьян, самка умирает вскоре после того, как прекратился репродуктивный период. Продолжительность жизни женщин вдвое больше, чем самок обезьян, за счет того, что пострепродуктивный период жизни сильно растянут. К. Льюис предполагает, что продолжительность жизни людей увеличилась ради обеспечения передачи знаний молодому поколению. По данным Б. Пеннинкса и других, есть корреляция между смертностью и психологическими факторами, такими, как утрата эмоциональной поддержки со стороны окружающих и сознание того, что человек уже не может быть хозяином своей судьбы.
В рамках концепции феноптоза это означает, что сигнал смерти, включающийся у старых обезьян после потери детородной способности, у женщин не возникает или не принимается организмом к исполнению, пока наличествует эмоциональная поддержка. Остается неясным, какие биохимические механизмы отвечают за такого рода регуляцию продолжительности жизни. Тем не менее очевидно, что факторы психологического порядка могут вызвать «биохимическое самоубийство» человека. Пожалуй, наиболее демонстративным примером служит так называемая «смерть вуду», когда человек умирает под действием внушения. Подобные ужасные случаи неоднократно описаны исследователями дикарей. Х. Истуол обсуждает два примера «смерти вуду» среди австралийских аборигенов, отмечая, что сильнейшее обезвоживание убивает человека, «проклятого» жрецом, в течение нескольких дней. В одном из упомянутых случаев врачебная помощь пришла слишком поздно, в другом женщину удалось спасти, увезя ее из мест обитания племени.
Общеизвестны примеры заболевания людей, иногда со смертельным исходом, при потере близкого человека. Зачастую болезни эти - вовсе не психического характера, а все те же инфаркт, инсульт или рак. Такого же рода случаи известны и среди домашних животных, которые иногда не в состоянии перенести смерть хозяина.
Вообще, феноптоз у людей можно рассматривать как вредный атавизм. В дикой природе феноптоз полезен прежде всего для выживания и эволюции сообществ организмов в агрессивных условиях среды. Люди устраивают свою жизнь так, чтобы свести к минимуму зависимость от внешних условий. Что касается эволюции, то мы давно уже не полагаемся на ее медленный темп. Чтобы взлететь, человек построил самолет, а не ждал миллионы лет, когда у него за спиной вырастут крылья.
Даже такая функция феноптоза, как очистка сообщества от мутантного потомства старых родителей, может быть заменена, скажем, законом, запрещающим иметь детей начиная с некоторого критического возраста. На смену самурайским традициям, управлявшим в течение длительного времени японским обществом, пришли в конце концов более гуманные законы.
Заключение
Предположение о запрограммированной смерти организма, выдвинутое Вейсманом более века назад, может быть по достоинству оценено только сегодня, когда уже описаны феномены самоликвидации внутриклеточных органелл - митохондрий, а также клеток (кстати, в октябре 2002 года С. Бреннеру, Дж. Э. Салстону и Х. Р. Хорвицу была присуждена Нобелевская премия за открытие механизма апоптоза) и органов. Явления же, относящиеся к категории феноптоза, прослежены на различных уровнях организации жизни. Однако на сегодня наших знаний недостаточно, чтобы сделать окончательный выбор между двумя концепциями старения, обсуждающимися со времен Вейсмана: смерть от старости как результат накопления случайных поломок или включения программы самоубийства. Но эти концепции, обычно рассматривающиеся как альтернативные, окажутся взаимодополняющими, если принять, что накопление поломок запускает программу самоубийства задолго до того, как поломки станут несовместимыми с жизнью организма.
В любом случае концепция феноптоза имеет одно очевидное преимущество перед альтернативной точкой зрения, исповедуемой подавляющим большинством геронтологов. Она допускает резкое увеличение продолжительности активной жизни, а в пределе - и отмену старения как такового. Для этого нам достаточно было бы выключить сигналы, вызывающие старение, или сломать механизм их реализации. Такие цели обретут черты реальности, когда мы узнаем природу сигналов и механизмов, о которых идет речь. Что же до традиционной концепции накопления поломок, то она вряд ли может обещать что-нибудь существенное, так как, исправив сегодня одну поломку, завтра мы столкнемся с другой, также требующей исправления.