Узбекские ученые работают над эликсиром вечной молодости (Герофитол, Тортезин)
Создание ранее казавшегося нереальным эликсира молодости (Герофитол) - дело техники, времени и кропотливой работы.
Именно так считают специалисты Института химии растительных веществ имени академика Юнусова. Долгое время они вели работу по поиску и дальнейшему внедрению в жизнь препарата, который мог бы остановить старение организма. По словам ведущего научного сотрудника института Ларисы Межлумян, это средство уже найдено, и называется оно «Герофитол».
Лариса Межлумян сообщила, что сейчас препарат проходит разного рода испытания, подвергается экспериментам. Это волшебное средство на самом деле способно продлить молодость человека, увеличить длительность жизни, добавить бодрости и сил.
Интересно, что подобного рода разработки и открытия не в новинку для отечественных ученых. Несколькими годами ранее специалисты Института биохимии Академии наук Узбекистана создали препарат Тортезин, на основе крови среднеазиатских черепах. К его свойствам относится способность дарить человеку долголетие, укреплять иммунную систему, а также бороться с воздействием радиации. Также средство рекомендуется для людей с анемией.
-----------------------
Изучение геронтопротекторного действия препарата Тортезин
Фомина Марина Александровна
аспирант, магистр биологии
Институт биохимии АН РУз, Ташкент, Узбекистан
E-mail: fominmarina@yandex.ru
В 2003-2004 г в Узбекистане был разработан новый иммуностимулирующий, радиотерапевтический и антианемический препарат «Тортезин». Препарат представляет собой сумму нейтральных олигопептидов из крови среднеазиатских черепах Testudo horsfieldi . Его планируется применять с целью профилактики и лечения людей, страдающих гематологическими заболеваниями различной этиологии, в частности иммунодефицитными состояниями, и для восстановления кроветворения после лучевой терапии. Разработан технологически простой способ получения крови черепах, не требующий умерщвления животных, и произведено патентование этого способа.
Доклинические испытания препарата на добровольцах (из числа разработчиков) выявили несколько очень приятных «незапланированных» эффектов. С первых дней после применения препарата наблюдалась нормализация сна, резкое улучшение мышечного тонуса, выносливости, возрастание половой активности. Так как не наблюдалось повышения аппетита, создаётся впечатление, что Тортезин нормализует, оптимизирует внутренние биохимические процессы в клетках, не используя внешние ресурсы.
Одной из актуальных проблем геронтологии является выяснение молекулярной основы физиологических механизмов старения и создание на этой основе комплексов мероприятий по увеличению продолжительности жизни. Значительное внимание уделяется роли пептидной регуляции старения. Считается, что современные гериатрические средства должны осуществлять нормализующее влияние на лимитирующие звенья процесса старения - генетический аппарат клеток, состояние клеточных биомембран, свободно- радикальные процессы (перекисное окисление липидов), энергетическое обеспечение клетки, систему микросомального (монооксигенезного) окисления, нейроэндокринную регуляцию.
Мы изучали влияние Тортезина (однократная иньекция, 1 мкг/кг массы) на продолжительность жизни беспородных белых мышей, поедание корма и общий тонус согласно общепринятым методическим рекомендациям.
Установлено, что Тортезин обладает ярко выраженным геронтопротекторным эффектом. Продолжительность жизни самцов увеличилась на 30%, самок - на 18%. Двигательная активность самцов на протяжении всего эксперимента составляла 250-300% к контролю, самок - 350-400%. Нагрузочные тесты (вращающийся стержень) показали увеличение работоспособности самцов в среднем на 160%, а у самок на 80%. Поедание корма при этом увеличилось у самцов всего на 35%, а у самок - на 15%.
-------------
РЖ ВИНИТИ 34 (MD00) 99.01-5929
Гемо- и иммуностимулирующий эффект экстракта клеток крови среднеазиатской черепахи [Текст] : научное издание / А. А. Турдыев [и др.] // Радиац. биол. Радиоэкол. - 1998. - Т. 38, N 2. - С. 207-214 . - ISSN 0869-8031
Аннотация: На пострадиационную терапевтическую эффективность проверены препараты из основных органов и тканей среднеазиатской черепахи - животного, известного своей феноменальной радиорезистентностью. Показано, что наряду с такими известными ранее веществами, как плазма, экстракты селезенки (ЭСЧ), взрослой и эмбриональной печени, экстракты из почек и мышц также способствуют увеличению выживаемости обученных мышей. Особенно значителен эффект экстракта цитозоля клеток крови, названного авторами "Тортезин". Его удельная активность в 4, а выход в 12 раз выше, чем у ЭСЧ при равной эффективности. Фактор увеличения дозы (ФУД) достигает 1,41. Экстракт обладает также заметной иммуностимулирующей активностью. Получена подробная физико-химическая характеристика "Тортезина", достаточная для его идентификации. Узбекистан, Ин-т биохимии АН, Ташкент. Библ. 22
| ГРНТИ | |
| УДК |
.
.
.
Угнетенное кроветворение - одно из наиболее серьезных последствий радиационного облучения человека. Поэтому в терапии лучевых поражений чрезвычайно важную роль играют процедуры и лекарственные средства, способные восстановить кроветворные функции организма. Для этого применяют пересадку костного мозга, переливание крови, а также препараты, приготовленные на основе экстрактов разных органов и тканей животных: тимуса, селезенки, печени, костного мозга.
В попытках получить наиболее эффективные средства для радиотерапии исследователи обратили внимание на животных, чей организм особенно устойчив к облучению. В этом отношении очень интересна среднеазиатская черепаха ( Testudo horsfieldi ) с ее феноменальной радиорезистентностью. Предполагается, что существует корреляция между этим свойством и терапевтической эффективностью препаратов, полученных из органов и тканей таких малочувствительных к радиации животных.
Группа сотрудников Института биохимии АН Республики Узбекистан изучала влияние водных экстрактов тканей, жидкостей и органов среднеазиатской черепахи на кроветворение (гемопоэз) у лабораторных облученных мышей. В экспериментах использовали кровь, желчь, мышцы, селезенку, почки и печень (в том числе эмбриональную), т.е. фактически все то, что традиционно применяли эскулапы со времен Авиценны. Эффективность полученных по оригинальной методике препаратов оценивали по фактору увеличения дозы (ФУД) облучения, которая вызывает пострадиационные поражения или гибель подопытных мышей.
В ходе испытаний установлено, что максимальным терапевтическим действием обладали экстракты эмбриональной печени, селезенки и клеток крови черепахи. Величины ФУД составляли для них соответственно: 1.46, 1.45 и 1.41; для экстракта печени взрослой черепахи - 1.10, мышц и почек еще ниже, а для желчи даже меньше единицы. Примечательно, что эффективность действия цитозоля черепахи (содержимого эритроцитов) по фактору увеличения дозы оказалась существенно выше в сравнении с препаратами, полученными из крови крыс (1.03) и человека (1.05). Это подтверждает гипотезу о корреляции между радиорезистентностью животных и противолучевой эффективностью вытяжек из их органов и тканей.
На основе цитозоля клеток крови черепахи узбекские исследователи создали противолучевой препарат "Тортезин". Его инъекции облученным мышам стимулируют рост численности стволовых клеток, что способствует восстановлению кроветворных функций организма. Препарат обладает также иммуностимулирующим эффектом. "Тортезин" прост в получении, а главное, относительно доступен: доля крови от массы черепахи достигает 4.2% осенью и 6.0% весной. Для сравнения: масса селезенки составляет 0.12% и 0.20%, печени - 3.7 и 5.3% у взрослой черепахи. В эритроцитах 82% составляет гемоглобин, но как показали исследователи, пострадиационную терапевтическую активность определяет не он, а, видимо, низкомолекулярные пептиды, имеющиеся в эритроцитах.
.
ИНСТИТУТ БИОХИМИИ
На правах рукописи
УДК 599. 591. 044; 612. 017. 1
НАЗИРОВА ЭЛЬМИРА РАХИМБЕРДИЕВНА
БИОХИМИЧЕСКИЕ И ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА ПРЕПАРАТА ТОРТЕЗИН
03.00.04. - биохимия; 14.00.25 - фармакология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата биологических наук
Т ашкент - 2012
ашкент - 2012
Работа выполнена в лаборатории радиационной биохимии и цитологии Института биохимии АН РУз.
Научные руководители: кандидат биологических наук
Александров Виталий Витальевич
кандидат биологических наук
Выпова Наталья Леонидовна
Официальные оппоненты: доктор медицинских наук, профессор
Сыров Владимир Николаевич;
кандидат биологических наук
Садыков Эркин Саодатович
Ведущая организация - Национальный Университет Узбекистана им. Мирзо Улугбека
Защита состоится « » ___________ 2012 г. в ______ часов на заседании Специализированного Совета Д 015.16.01 по защите диссертаций на соискание ученой степени доктора наук при Институте биохимии Академии Наук Республики Узбекистан по адресу: 100125, Ташкент, ул. Х. Абдуллаева, 56.
С диссертацией можно ознакомиться в библиотеке Института биохимии АН РУз.
Автореферат разослан «_____» ___________ 2012 г.
Ученый секретарь
Специализированного Совета,
к андидат биологических наук Г.У.Усманова
андидат биологических наук Г.У.Усманова
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность работы. В последнее время наблюдается настоящий всплеск интереса к внедрению прошедших многовековую проверку средств народной медицины (растительного, минерального и животного происхождения) в медицину официальную. Политика ВОЗ направлена на поддержку клинических исследований безопасности и эффективности средств народной медицины и на пропаганду их рационального использования (Стратегия ВОЗ,2001). В настоящее время в традиционной китайской медицине используется более 1500 продуктов животного происхождения (Advanced Textbook..,1995); в аюрведической медицине до 20% рецептов основано на животных субстанциях (Unnikrishnan, 1998); в Бразилии более 180 животных имеют медицинское применение (Alves R., Rosa I., 2005). В традиционной европейской медицине также существуют лекарства из сырья животного происхождения - органопрепараты. К ним относят получаемые из органов и тканей животных формы, действующими веществами которых являются продукты физиологического обмена, содержащиеся или накапливающиеся в органах, тканях, биологических жидкостях (Гуров В.А.,1976; Чуешов В.И., 2002). Современные органопрепараты являются преимущественно комплексами натурального происхождения и сложного состава; наиболее многочисленны препараты крови и тимуса.
Многие виды пресмыкающихся существуют в практически неизменном виде сотни миллионов лет, сохранив эволюционно удачные биохимические механизмы. Ключи к некоторым из этих механизмов могут запустить подобные механизмы у млекопитающих. Поэтому использование рептилий в лечебных целях имеет многовековую историю. Биохимические факторы, выделенные из змей, черепах и крокодилов, оказывают на млекопитающих свое сильное антибактериальное, иммуностимулирующее и антианемическое действие (Merchant, 2006). Из селезенки среднеазиатской черепахи Testudo horsfieldi выделен, расшифрован и запатентован в России и США тетрапептид «Phe-Thr-Gly-Asn», вызывающий стимуляцию гемопоэза млекопитающих (Turdiev A., 2007). Как потенциальный источник сырья для лекарственных препаратов, среднеазиатская черепаха имеет ряд неоспоримых преимуществ перед другими рептилиями. Она распространена повсеместно (Bonnet X., Lagarde F., 2001), неприхотлива при содержании и искусственном размножении.
Получаемый из крови весенних черепах полипептидный препарат Тортезин попадает под определение органопрепарата, по составу и действию близкому к препаратам тимуса.
Степень изученности работы. В Институте биохимии АН РУз с 1980-х годов ведутся исследования механизмов феноменальной устойчивости рептилий к экстремальным воздействиям, и влияния биогенных факторов рептилий на млекопитающих (Маджидова Д.Х., 1982; Усманов Р.Б., 1986; Прус Е.К., 1990; Александров В.В., 1996; Турдыев А.А. и др., 1998; Тагайалиева Н.А., 2002). На основе этих факторов в 2003-2008 гг. был разработан новый иммуностимулирующий и радиотерапевтический препарат Тортезин. Препарат представляет собой сумму нейтральных олигопептидов из крови среднеазиатских черепах Testudo horsfieldi . Его предлагается применять для профилактики и лечения людей, страдающих гематологическими заболеваниями различной этиологии, в частности иммунодефицитными состояниями, и для восстановления кроветворения после лучевой и химиотерапии. Была разработана технология получения крови черепах без их умерщвления, создана инъекционная лекарственная форма в виде стерильного лиофилизата с наполнителем, и изучены её некоторые биологические эффекты (Фомина М.А., 2008). Предварительные опыты показали высокую эффективность Тортезина на ряде модельных систем. Для дальнейшего внедрения нового препарата в практику остро встал вопрос о проведении в полном объёме соответствующих исследований.
Связь диссертационной работы с тематическими планами НИР. Работа выполнена в рамках проектов П-15.45 «Разработка иммуностимулирующего и радиотерапевтического препарата нового типа», А-10-067 «Разработка препарата для профилактики и лечения анемии» и ФА-И1Т 028 И-109 «Освоение технологии производства субстанции препарата Тортезин».
Цель исследования: изучение биохимических и фармакологических свойств лекарственной формы препарата Тортезин и проведение соответствующих исследований в объёме, достаточном для получения разрешительных документов Фармакологического Комитета Республики Узбекистан.
Задачи исследования:
-
Разработать подходы к биохимической стандартизации субстанции и лекарственной формы. Изучить действие Тортезина на метаболические процессы. -
Провести доклиническое изучение токсикологии и фармакологии препарата. -
Провести клиническую проверку безопасности (переносимости). -
Расширить перечень рекомендуемых областей применения препарата.
Объект и предмет исследования: лекарственная форма препарата Тортезин из крови черепахи экспериментального производства Института биохимии АН РУз.
Методы исследований. Флуоресцентная спектроскопия, электрофорез, HPLС-хроматография, фармакологические, иммунологические, цитологические и гематологические методы.
Основные положения, выносимые на защиту:
Разработанные для ВФС биохимические показатели и методы анализа;
Результаты комплексного изучения фармакологии и токсикологии лекарственной формы препарата Тортезин.
Результаты клинической проверки безопасности препарата.
Результаты исследований по расширению перечня рекомендуемых областей применения.
Научная новизна. Впервые исследованы возможности оптических, электрофоретических и хроматографических методов для стандартизации препарата. Изучена корреляция между уровнем оксида азота и процессами метаболизма в интактном организме под действием препарата. Проведено доклиническое изучение токсикологии и фармакологии препарата Тортезин, проведена клиническая проверка безопасности препарата, экспериментально установлены его антианемическое и стресс-протекторное действия; показано положительное влияние препарата на половую функцию.
Научная и практическая значимость результатов исследования.
Результаты исследования расширяют рекомендуемые области применения препарата, что открывает перспективы коррекции некоторых гематологических и соматических заболеваний.
Реализация результатов. На основании представленных материалов Фармкомитет РУз выдал разрешение 29/03-382 от 1.04.2010 на проведение 2-й фазы клинических испытаний препарата Тортезин (проверка эффективности).
Апробация работы. Материалы диссертации представлены или доложены на: Конференции «Мустакиллик йилларида илм-фан тараккиёти: мухим фундаментал натижалар, амалий ютуклар ва инновациялар», Ташкент, 2011; Первой международной научно-практической конференции «Высокие технологии, фундаментальные и прикладные исследования в физиологии и медицине», Санкт-Петербург,Россия, 2010; конференции «Клиническая иммунология, иммуногенетика - междисциплинарные проблемы», посвященной 25-летию Института иммунологии АН РУз, Ташкент, 2010 год; международной научной конференции «Актуальные проблемы развития биоорганической химии», Ташкент, 2010 год; XV Международной конференции студентов, аспирантов и молодых ученых «Ломоносов», Москва, 2008.
Опубликованность результатов. По теме диссертации опубликовано 11 работ, в том числе 7 журнальных статей.
Структура и объем диссертации. Диссертация изложена на 120 страницах машинописного текста и состоит из введения, трех глав (обзор литературы, материалы и методы, собственные исследования), заключения, выводов и списка цитируемой литературы, включающего 190 источников, в том числе 44 иностранных. Диссертация содержит 24 таблицы и 18 рисунков.
ОСНОВНОЕ СОДЕРЖАНИЕ ДИССЕРТАЦИИ
Материалы и методы исследования.
Использовалась лекарственная форма препарата Тортезин, в виде лиофилизированного порошка белого цвета в пенициллиновых флаконах на 10 мл, содержащих 100 мкг активного вещества и 80 мг маннита, экспериментального производства Института биохимии АН РУз. Препарат Тортезин в дозах 1, 2,5 и 5 мкг/кг вводили внутримышечно, исследования проводили через 10 дней и 1 месяц после введений. Исследования проведены на половозрелых мышах-самцах линии СВА и белых беспородных мышах-самцах массой 18-22 г., белых беспородных крысах массой 200-240 г., а также кроликах породы «Шиншилла» массой 3,0-3,5 кг. Всего было использовано 40 мышей, 60 крыс, 24 кролика и 30 морских свинок. Резистентность эритроцитов определяли по Лимбеки и Рибьера in vivo и in vitro . Для регистрации процесса свертывания крови был применен метод тромбоэластографии. Для исследования антистрессового действия применяли модель нервно-мышечного напряжения по Селье (Селье Г., 1972).
Количество эритроцитов измеряли на гематологическом анализаторе «Abacus Junior», Австрия, по рекомендациям фирмы-производителя.
Оксид азота (NO) определяли фотометрически при 546 нм реактивом Грейса (Звягина Т.В. и др., 2001). Перекисное оксиление липидов (ПОЛ) в сыворотке крови определяли по содержанию первичных продуктов этой реакции - диеновых и триеновых коньюгатов (ДК и ТК) и определение конечного продукта - малонового диальдегида (МДА) - по реакции между МДА и тиобарбитуровой кислотой с образованием окрашенного триметинового комплекса (Каган B.E и др., 1986; Климов А.Н., Никулочева Н.Г., 1999). Содержание молочной кислоты (МК) определяли по методу Хохорста, содержание пировиноградной кислоты (ПВК) - по методу Цока и Лампрехта (Методы биохимических исследований, 1982).Достоверность оценивалась по критерию χ-квадрат.
Флуоресцентная спектроскопия препарата Тортезин проведена на спектрофотометре Hitachi F-4500 (Япония) при комнатной температуре в диапазоне от 320 до 550 нм. Электрофорез препарата осуществлен в 10% полиакриламидном геле при денатурирующих условиях в присутствии SDS-Na по Laemly (1970). Окрашивание фракций проводили серебром по Блюму и Кумасси голубым G-250 (Остерман Л.А.,1981). Обратнофазовая HPLC выполнена с использованием колонок SYMMETRY-300 C18. Фракции после хроматографических разделений лиофильно высушивали и хранили при температуре - 20°С.
Клинические исследования препарата проведены в РОНЦ МЗ РУз в отделении химио- и лучевой терапии. В исследование были взяты больные, находящиеся на стационарном лечении. В группах, получивших исследуемый препарат, было 15 больных с неходжкинскими лимфомами и 15 больных с опухолями малого таза. В контрольных группах также было по 15 больных с неходжкинскими лимфомами и 15 больных с опухолями малого
таза. В исследование включались больные обоего пола в возрасте от 18 до 70 лет, давшие письменное информированное согласие на включение в исследование. Больные, получившие курс химио- и лучевой терапии, на фоне основного лечения получили однократно Тортезин в дозе 50 мкг/м2 внутримышечно в день начала лечения. Определение клинических показателей у больных всех групп проводилось в первый день начала терапии и через 3 недели после ее завершения.
ОСНОВНЫЕ РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ
И ИХ ОБСУЖДЕНИЕ
Биохимическая стандартизация субстанции Тортезина
При выборе показателей ВФС и методов анализа учитывалось, что эти показатели и методы должны служить не полному анализу всех свойств препарата, а лишь установлению факта, что по своим качествам он будет соответствовать требованиям НД, гарантирующим его биологическое действие и свойства.
Удельный показатель поглощения. Спектрофотометрические методы исследования биологически активных веществ постоянно используются при их идентификации (Ковалева С.В. и др.,1988, 2002; Евтушенко Н.С. и др., 2003). УФ-спектр водного раствора субстанции не имеет выраженных максимумов (рис.1), а имеет яркий пик пептидной связи при 218 нм, и небольшой подъём при 284 нм (ароматические аминокислоты).
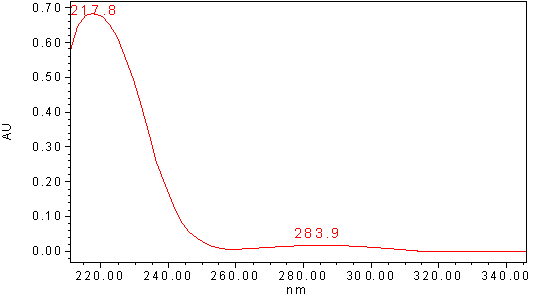
Рис.1. УФ-спектр (210 - 350 нм) поглощения водного раствора 500 мкг/мл субстанции Тортезина.
Для ВФС был рекомендован удельный показатель поглощения при 218 и 284 нм.
Хроматография . Для характеристики всех компонентов Тортезина исследовали возможности метода HPLC - обращено-фазовой жидкостной хроматографии при высоком давлении. Эксперименты показали полную применимость этого метода. Тортезин выходит тремя основными фракциями - на 2-12 мин, на 12-23 мин и на 23-31 мин. Особенно ярко это проявляется при наложении профилей элюции друг на друга (рис.2). Для идентификации можно взять одинаковые пики, выходящие (при данных условиях) на 5, 8 и 16 мин.
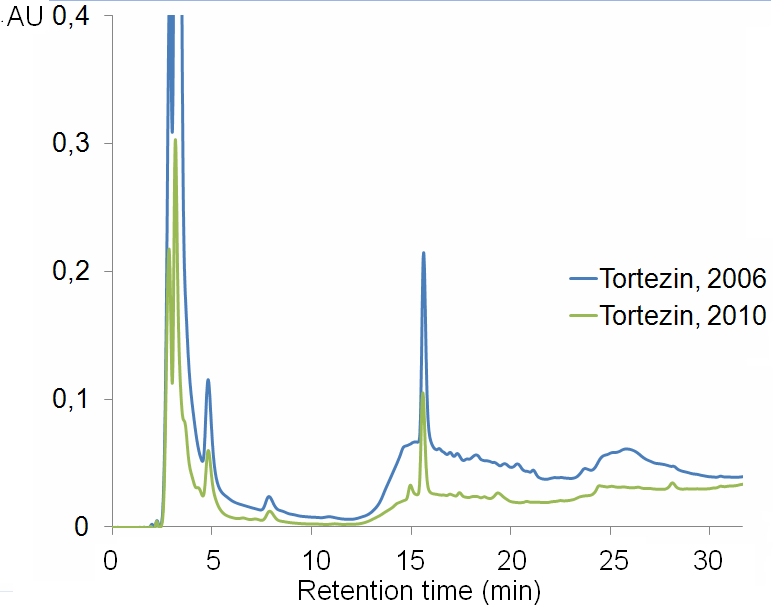
Рис. 2. HPLC Тортезина. Детекция при 280 нм. Наложение разделений 2006 и 2010гг.
Таким образом, для определения подлинности Тортезина предложена хроматография на обращено-фазовых С18 носителях с детектированием при 280 нм.
Биохимическая стандартизация лекарственной формы Тортезина
Ультрафильтрация. Главная сложность стандартизации лекарственной формы Тортезина связана с наличием наполнителя - маннитола. Необходимость наполнителя была установлена на этапе разработки лекарственной формы. На 100 мкг субстанции каждый флакон содержит 8 мг наполнителя. Для стандартизации лекарственной формы пригодным оказался метод ультрафильтрации. Мы использовали ультрацентрифугирование препарата с помощью ультрамембраны Viva Spin 4, 5000MWCO PES (Sartorius Group, UK) при 3000об/мин. По результатам гельфильтрации субстанции Тортезина заметная часть Тортезина состоит из низкомолекулярных компонентов. При ультрафильтрации через мембрану с пороговым значением 10 кДа эти низкомолекулярные компоненты будут потеряны вместе с наполнителем. Зато ультрафильтрат обогатится более тяжелыми компонентами, что теперь делает возможным применение электрофоретических методов. (Ранее из-за огромного количества наполнителя использование электрофореза было невозможным).
Электрофорез. Исследовали образцы двух серий препарата: 2007 и 2010 гг. (рис. 3 и 4).
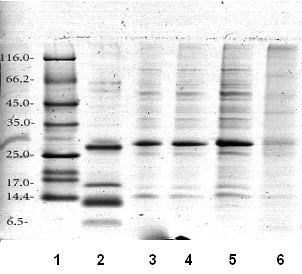
Рис. 3. Электрофорез в 10% ПААГ. Окрашивание Кумасси G250.
1 - белковые маркеры (Mr - 14.4-116 кДа)
2 - пептидные маркеры (Mr-1.06- 26.6 кДа)
3 - Тортезин, 2010г., 5 мкл 1мг/мл
4 - Тортезин, 2010г., 10 мкл 1мг/мл
5 - Тортезин, 2007г., 20 мкл 1мг/мл
6 - Тортезин, 2007г., 10 мкл 1мг/мл

А |

Б |
Рис. 4. Электрофорез в 10% ПААГ. Окрашивание серебром.
1 - белковые маркеры (Mr - 14.4, 18.4, 25.0, 35.0, 45.0, 66.2, 116.0 кДа)
2 - пептидные маркеры (Mr-1.06, 3.5, 6.5, 14.2, 17.0, 26.6 кДа)
3 - Тортезин, 10 мкл 1мг/мл
А - Тортезин, 2007 г. 1 - белковые; 2 - пептидные маркеры
Б - Тортезин, 2010 г. 1- пептидные; 2 - белковые маркеры
При окрашивании Кумасси G-250 препаратов 2007 и 2010 гг. (рис. 3) выявляется более 20 зон белковых фракций, лежащих в области высоко- и низкомолекулярных компонентов. Не обнаруживается различие в качественном составе белковых зон препаратов 2007 и 2010 гг., что говорит о том, что биологическая активность препарата сохраняется в течение 3х лет.
При окрашивании электрофореграмм ионами серебра получается более четкое разделение препарата (рис.4).
Действие лекарственной формы препарата Тортезин на метаболические процессы
Оксид азота (NO) - универсальный аутокринный и паракринный медиатор, имеющий в организме множественные функции. Как избыток, так и дефицит оксида азота неблагоприятен для организма. Для оценки потенциальных побочных эффектов использования нового препарата изучали влияние Тортезина на уровень оксида азота (рис.5).

Рис. 5. Содержание оксида азота в сыворотке крови интактных крыс после в/м инъекции Тортезина в динамике (М ± m, % к контролю)
Через 1 час после введения Тортезина уровень оксида азота резко возрастает до 150-160%, что говорит о несомненном действии препарата на систему NO-синтеза. Через 24 часа уровень NO фактически возвращается к норме (94±5 %) и далее достоверно не меняется. Теоретически это говорит о потенциальном гипотензивном действии препарата в первый час после введения. Однако (по нашим наблюдениям) артериальное давление ни через час, ни в первые 72 часа не меняется.
Учитывая множественные медиаторные свойства NO в первые часы после введения Тортезина, можно ожидать усиления метаболических процессов в организме. В этой связи была изучена корреляция между уровнем NO и процессами метаболизма (ПОЛ, гликолиз и углеводный обмен) у интактных крыс под действием препарата Тортезин не вызвал достоверного изменения уровня всех определявшихся продуктов ПОЛ. Однако к 72 часам их содержание несколько снизилось и достигло 89, 97 и 80% для МДА, ДК и ТК соответственно. Это можно рассматривать как отсутствие деструктивных процессов в тканях в изучавшиеся сроки и в целом как положительную динамику (табл.1).
Таблица 1.
Влияние Тортезина на ПОЛ (МДА, ДК и ТК) в сыворотке крови у интактных крыс в динамике ( Мm; n=5)
Препарат |
Время исслед. часы |
МДА |
ДК |
ТК | |||
нмоль/мл |
% |
нмоль/мл |
% |
нмоль/мл |
% | ||
Контроль |
11,74±1,0 |
100 |
1,61±0,1 |
100 |
0,24±0,02 |
100 | |
|
Тортезин |
1 |
11,3±1,1 |
97 |
1,66±0,1 |
103 |
0,24±0,02 |
100 |
24 |
12,0±1,6 |
103 |
1,60±0,1 |
100 |
0,26±0,02 |
104 | |
48 |
11,2±1,8 |
96 |
1,58±0,1 |
98 |
0,22±0,02 |
88 | |
72 |
10,4±1,3 |
89 |
1,56±0,1 |
97 |
0,20±0,02 |
80 | |
МК и ПВК можно рассматривать как более надежные индикаторы углеводного обмена, чем уровень глюкозы, который является чрезвычайно лабильным (Камышников В.С., 2004). Как следует из табл. 2, введение Тортезина привело к определенному возрастанию этих метаболитов к 72 ч до 118 и 124% для МК и ПВК соответственно, что может быть расценено как усиление гликолиза.
Таблица 2.
Влияние Тортезина на гликолиз (МК) и углеводный обмен (ПВК) в сыворотке крови у интактных крыс в динамике ( Мm; n=5)
Препарат |
Время исслед. часы |
МК |
ПВК | ||
мкмоль/мл |
% |
мкмоль/мл |
% | ||
Контроль |
3,04±0,2 |
100 |
89,5±5,6 |
100 | |
|
Тортезин |
1 |
2,92±0,2 |
96 |
80,4±4,7 |
89 |
24 |
3,06±0,2 |
100 |
92,6±6,0 |
103 | |
48 |
3,14±0,2 |
103 |
102,07±7,4 |
114 | |
72 |
3,6±0,2 |
118* |
111,3±8,4 |
124* | |
*Р 0,05 по отношению к контролю
Таким образом, не наблюдается прямой корреляции между повышенным уровнем оксида азота под действием Тортезина через 1 ч после инъекции и активацией метаболических процессов. Тортезин вызывает умеренное усиление гликолиза через 72 ч после введения, не вызывая достоверного изменения процессов ПОЛ.
Изучение фармакотоксикологии препарата Тортезин
Целью токсикологических исследований нового фармакологического вещества является установление характера и выраженности его повреждающего действия на организм экспериментальных животных и оценка его безопасности. Вид необходимых исследований, их объём и порядок проведения определяются нормативными документами в зависимости от принадлежности потенциального препарата к соответствующей категории.
Изучение острой токсичности лекарственной формы Тортезин было проведено в полном объёме в соответствии с «Инструкция по доклиническому испытанию» (2000); (Саноцкий И.В.,1970). Были изучены острая и хроническая токсичность, кумулятивное действие, местно-раздражающее действие, аллергизирующие свойства и действие препарата Тортезин на гемолиз эритроцитов и процессы свертывания крови.
Исследования показали, что препарат относится к классу малотоксичных соединений. LD50 - более 1000 мг/кг при внутримышечном и пероральном введении на мышах и крысах. Тортезин не обладает кумулятивным действием. При ежедневном внутримышечном многократном введении препарат Тортезин не оказывает влияния на поведение и динамику веса животных. Препарат не оказывает токсического действия на функцию почек и печени, а также на патоморфологию органов и тканей животных. Тортезин не обладает местно-раздражающим и аллергенным действием.
Таким образом, препарат не оказывает токсического действия на организм животных.
Изучение общей фармакологии препарата Тортезин
Исследования общей фармакологии препарата показали, что Тортезин в дозе 0,01 мг/кг не влиял, а в дозе 0,05 мг/кг оказывал незначительное прессорное действие в острых опытах на кошках, не влияя на деятельность сердца, не оказывая влияния на подтипы адрено-, М- и Н-холинорецепторов. Тортезин оказывал двухфазное влияние на двигательную активность интактных белых мышей: в первый день несколько угнетал её, особенно от больших доз, а на вторые сутки активировал её. В первый день после введения Тортезин удлинял снотворный эффект этаминала - натрия, а также оказал незначительное противосудорожное действие на фоне коразоловых судорог, в то время как на следующий день после введения на фоне активации спонтанной двигательной активности Тортезин незначительно усиливал судорожное действие коразола. Было замечено, что активирующее действие Тортезина в дозе 0,05 мг/кг на следующий день после введения сопровождалось усиленным приёмом пищи, по сравнению с контрольной группой мышей. На изолированном кишечнике кроликов отмечалось активирующее действие препарата на деятельность органа. Препарат нормализует общий тонус организма, продлевает и улучшает качество жизни, благотворно влияет на нервно-психический статус.
Побочных эффектов препарата не обнаружено.
Клиническое исследование препарата Тортезин
Решением расширенного заседания Фармакологического комитета (протокол № 3 от 14.12.2007г.) Тортезин был допущен до клинических испытаний как средство сопровождения лучевой и химиотерапии. В 2009 г. в РОНЦ МЗ РУз было проведено клиническое исследование по изучению протекторного действия и переносимости препарата Тортезин при полихимиотерапии больных с неходжкинскими лимфомами и при лучевой терапии больных с опухолями органов малого таза для выявления возможности рекомендации клинического применения препарата в Республике Узбекистан. При формировании перечень значимых клинических показателей (Флетчер Р.,1998) включал в себя преимущественно основные биохимические параметры крови и иммунологические характеристики - лейкоциты крови; В- и Т- лимфоциты крови; CD4+ и CD8+ лимфоциты (Т-хелперы и Т-супрессоры).
Не было отмечено ни одного случая жалобы или недомогания, связанных с препаратом. В первые дни после инъекции более 25% пациентов отмечали улучшение общего самочувствия и возрастание физической активности.
Анализ иммунологических характеристик, определенных перед лечением и через 3 недели после завершения лечения, показал, что влияние препарата Тортезин на эти показатели отсутствует. К аналогичному выводу приводит и сравнение результатов биохимических анализов в группах. Попарное сравнение однотипных выборок для опытных и контрольных групп показало, что с вероятностью более 95% они относятся к одним генеральным совокупностям. Таким образом, хотя у части больных отмечается заметное изменение ряда параметров, достоверные статистические отличия между группами не выявлены.
Эффективность лечения (табл.3) оценивалась по 4-х балльной шкале в соответствии с Протоколом исследования и включала наряду с изменением данных лабораторных исследований изменение общего состояния пациентов (клинический эффект и качество жизни).
Таблица 3.
Влияние препарата на эффективность и переносимость лечения,
М±m, Р≤ 0,05
|
Показатель |
В процессе лечения | |||
контроль |
Тортезин | |||
лучевая терапия |
химиотерапия |
лучевая терапия |
химиотерапия | |
Эффективность (макс. 4 балла) |
3,4± 0,5 |
2,5±0,5 |
2,5±0,5 |
2,4±0,5 |
Переносимость (макс.5 баллов) |
3,5± 0,5 |
3,5±0,5 |
2,7±0,5 |
3,6±0,5 |
Переносимость лечения (табл.3) оценивалась врачом-исследователем по 5-ти балльной шкале в соответствии с Протоколом исследования на основании субъективных симптомов и ощущений, сообщаемых пациентом, и объективных данных, полученных в процессе лечения.
Достоверного (р ≥ 95%) влияния препарата Тортезин на эффективность и переносимость применявшегося лечения не выявлено. Также не удалось (р ≥ 95%) выявить корреляцию между группами по признакам пола, возраста и диагноза. Ясно, что применявшиеся виды лечения (лечение комбинацией цитостатиков при химиотерапии; дробное облучение в высокой дозе области таза при лучевой терапии) по своему характеру являются достаточно агрессивными, и вызывают подавление роста всех (а не только раковых) клеток. Поэтому ожидание, что на фоне подавления роста всех клеток использование препарата вызовет общее улучшение состояния, «смягчение» показателей и избирательную стимуляцию иммунной и гемопоэтической систем, не оправдалось.
Фармакологический Комитет Республики Узбекистан в марте 2010 г утвердил результаты проведенного клинического исследования.
Таким образом, проведенное клиническое исследование не выявило достоверных (р ≥ 95%) преимуществ одновременного применения препарата Тортезин и полихимиотерапии больных с неходжкинскими лимфомами, и дробно-лучевой терапии больных с опухолями органов малого таза, и показало хорошую переносимость инъекции препарата Тортезин.
Изучение антианемического действия препарата Тортезин
После установления безвредности препарата были проведены исследования, при которых у всех добровольцев, получивших 1 внутримышечную инъекцию препарата (1 мкг/кг), было отмечено повышение уровня гемоглобина. Результаты представлены в табл. 4. Средний объём эритроцитов составлял 63 фл. Через 1 месяц после инъекции средний объём вырос до 69 фл, а через 2 месяца - до 76 фл за счет появления молодых форм эритроцитов. Общее количество эритроцитов, уровень гемоглобина и количество гемоглобина в одном эритроците также возросли.
Таблица 4.
Некоторые показатели крови до и после применения Тортезина.
Показатели |
До эксперимента |
Через 1 месяц |
Через 2 месяца |
Гемоглобин |
83 |
114 |
115 |
Эритроциты, млн/мкл |
4,43 |
5,29 |
5,20 |
Гемоглобина в 1 эритроците, пг |
18,7 |
21,5 |
22,2 |
Средний объём эритроцита, фл |
63 |
69 |
76 |
Клетки объёмом 56 фл, % |
75,7 |
61,4 |
39,7 |
Клетки объемом 86 фл, % |
14,1 |
32,5 |
47,4 |
Компьютерный анализ гистограмм выявил, что до лечения популяция эритроцитов состояла из клеток двух типов - объёмом 56 и 86 фл; после лечения клеток новых типов не появилось, но изменилось соотношение между ними. Доля старых клеток снизилась с 75% до 40%; доля молодых возросла с 14% до 47% к концу второго месяца (две нижние строки в табл.4). Начиная со второго месяца, в крови появляется новый тип молодых эритроцитов, которые заметно крупнее по размеру, что характерно именно для молодых клеток.
Таким образом, по механизму действия Тортезин, подобно эритропоэтину, имеет несколько точек приложения, одновременно воздействуя как на иерархически высокие этажи кроветворения, т.н. «стволовые клетки», так и на процессы выброса молодых форм эритроцитов.
Антистрессовое и антидепрессивное действие Тортезина
Острый стресс сопровождается инволюцией тимуса, гипертрофией надпочечника и образованием язв на слизистой оболочке желудка. Полученные результаты представлены в таблицах 5 и 6.
Таблица 5.
Изменение веса животных и их органов у крыс со стрессом при профилактическом применении препарата Тортезин (n=6)
Органы |
Интактные жив. |
Контроль-стресс |
Тортезин-стресс | |||
М±m |
КМ* |
М±m |
КМ |
М±m |
КМ | |
Крыса, грамм |
220±20 |
- |
200±20 |
- |
202±20 |
- |
Селезенка, мг |
610±40 |
36 |
634±40 |
32 |
675±55 |
30 |
Тимус, мг |
180±15 |
110 |
135±12 |
114 |
215±20 |
86 |
Надпочечники, мг |
32±2 |
733 |
36±3 |
556 |
34±3 |
594 |
Почки, мг |
503±45 |
44 |
563±45 |
36 |
625±50 |
32 |
Гипофиз, мг |
12±1,0 |
1800 |
18±1,4 |
1111 |
12±1,0 |
1683 |
*коэффициент массы КМ = масса тела /массу органов животных х 100 .
Р 0,01 по отношению к контролю.
Таблица 6.
Протекторное действие препарата Тортезин на образование язв в желудке у крыс подвергшихся стрессу ( М±m; n=6)
Группы, препарат |
Количество эрозий |
Количество язв |
Крово- излия-ний |
Сумма пораж ений | ||
больших |
малых |
больших |
малых | |||
Интактная |
- |
- |
- |
- |
- |
- |
Контрольная-стресс |
1,0±1,0 |
1,5±1,0 |
1,8±1,0 |
1,5±0,1 |
0,5±0,04 |
6,3±0,4 |
Тортезин-стресс |
1±0,1 |
1,8±0,1 |
- |
- |
- |
2,8±0,2 |
Р 0,01 по отношению к контролю.
Введение за 48 часов до стресса опытным крысам препарата Тортезин в дозе 1 мкг/кг приводит к увеличению массы тимуса на 20% по отношению к интактным животным, и на 60 % - по отношению к контролю. Таким образом, инволюции тимуса не наблюдается. Также мы наблюдали уменьшение гиперплазии надпочечников. При этом вес почек под действием Тортезина был увеличен на 25% по отношению к интактным показателям. Вес гипофиза в опытной группе не отличался от веса у крыс интактной группы и был на 34% меньше, чем в контрольной группе (рис.5).
Введение препарата Тортезин за 48 часов до стресса привело к сокращению общего количества поражений желудка с 6,3±0,4 до 2,8±0,2 (табл.6). При этом у опытных крыс отсутствовали язвы и кровотечения, а были зарегистрированы только эрозии. Следовательно, происходит восстановление соматических показателей до нормы.
Исследования стресс-протекторного действия препарата Тортезин на лимфоидные органы и кровь крыс представлены в таблице 7.
Таблица 7.
Цитологические исследования костного мозга, лимфоидных органов и перитониальной жидкости у крыс после стресса
Группы |
Костный мозг, 106 |
Тимус, 106 |
Селезенка, 106 |
Моноциты, на 1 мл перитонеальной жидкости,% |
Интактная |
1507±100 |
146±10 |
5683±500 |
100±10 |
Контрольная-стресс |
1402±100 |
100±12 |
5332±400 |
143±12 |
Тортезин-стресс |
1744±120 |
140±12 |
7982±600 |
190±16 |
Р 0,01 по отношению к контролю.
Введение Тортезина за 48 часов до стресса привело к достоверному увеличению количества кариоцитов в костном мозге на 24% по отношению к контролю. Количество тимоцитов в опытной группе не отличалось от интактных животных. У опытных крыс увеличено количество макрофагов по сравнению с контролем на 33%, по отношению к интактной группе на 90%. Наряду с этим в опытной группе животных было увеличено количество спленоцитов в селезенке на 40%. Таким образом, у опытных крыс наблюдается повышенный иммунитет, что позволило им лучше перенести стресс по сравнению с контрольной группой.
Изучение влияния препарата Тортезин на морфологический состав периферической крови контрольной и опытной групп не показало достоверных различий между группами.
Эти данные, а также результаты теста «открытое поле» по оценке функционального состояния центральной нервной системы (ЦНС) у крыс, и оценка депрессии добровольцев по опроснику Бэка в течение 15 месяцев позволяют считать, что препарат Тортезин обладает выраженным стресс-протекторным и антидепрессивным действием на центральную нервную систему.
Влияние Тортезина на половую функцию
Исследования направлены на изучение новых точек приложения препарата Тортезин в медицинской практике.
Исследование по влиянию препарата на половую функцию крыс-самцов показало, что при введении Тортезина крысам в дозе 1 мкг/кг п/к за 4 часа до начала опыта число покрытий увеличилось на 48%, латентный период 1-й эякуляции укоротился на 25%, а число эякуляций увеличилось на 66% .
Продолжительное введение Тортезина в дозе 1 мкг на животное при введении 1 раз в неделю практически не повлиял на половое созревание и плодовитость крыс.
Изучение влияния некоторых коммерческих иммуностимуляторов и Тортезина, в рекомендуемых разработчиками диапазоне концентраций, на жизнестойкость и жизнеспособность сперматозоидов in vitro через 24 часа хранения при 4оС показало, что препараты тималин (Украина) и тимоген (Россия) из-за угнетающего эффекта не могут рассматриваться как средства, повышающие жизнестойкость сперматозоидов. Разработанные в Узбекистане тимоптин и иммуномодулин (оба препарата фактически имеют одинаковый состав - пептиды-регуляторы из тимуса с/х животных) обладают определенным стимулирующим действием на данной модельной системе, особенно иммуномодулин при дозе 1 мкг/мл - 197%. При этой же концентрации очень активен Тортезин - 164%.
ЗАКЛЮЧЕНИЕ
Важная особенность современного этапа стандартизации лекарственных средств (ЛС) - гармонизация требований к качеству ЛС и методам их испытаний, предъявляемых фармакопеей страны-производителя. Одной из целью настоящей работы был выбор подходящих биохимических методов для анализа нового препарата.
Темпы ежегодного прироста рынка ЛС составляет около 10% (Рейхарт Д.В., 2010). Параллельно происходит и обратный процесс - с рынка уходит огромное количество препаратов, не оправдавших надежды создателей. Важнейшим, решающим этапом в движении нового, потенциально перспективного препарата на рынок являются клинические испытания. «Проведение любого клинического испытания в соответствии с международными правилами - большой труд, требующий не только напряжения интеллекта, но и определенных затрат времени, сил и средств. Но взамен это дает настоящую науку, серьезную репутацию, возможность публиковать данные в ведущих международных журналах и спокойный сон» (Мелихов О.Г., Прудников Д., 1997). И важный шаг в этом направлении был нами сделан в настоящей работе.
Из литературы известно, что органы и кровь различных позвоночных могут служить источником препаратов самой различной направленности, в частности как регуляторов кроветворения. Это препараты тимуса, спленин из селезенки и миелопид, продуцируемый клетками костного мозга (Комиссаренко В.П., 1963; Способ получения миелопида, 1993), препараты из крови телят (Карякин А.В. и др., 1998), из акульей крови (Хауард М., 1997), человека (Фишман Пиина, 1997; Старцев В.Ф., 1998; Слабкая Е.В., 2000). Поэтому эмпирически обнаруженные эффекты Тортезина из крови черепахи (антианемический и влияние на половую функцию) не являются чем-то исключительным.
По нашему мнению, Тортезин является очень перспективным полифункциональным препаратом, способным занять свою «нишу» на фармацевтическом рынке. Его активность, по-видимому, связана не с отдельными ингредиентами, а с композиционными отношениями её составляющих, принимающих взаимодополняющее участие в формировании общей активности. Поэтому попытки выделить из субстанции «активное начало» едва ли принесут успех.
Если удастся объединить усилия разработчиков с интересами потенциального производителя - фармацевтической компании, - то появление Тортезина на прилавках аптек скоро станет реальностью.
ВЫВОДЫ
Для биохимической стандартизации субстанции препарата Тортезин рекомендованы удельный показатель поглощения при 218 и 284 нм и хроматография на обращено-фазовых С18 носителях с детектированием при 280 нм. Для биохимической стандартизации лекарственной формы препарата Тортезин рекомендовано сочетание методов ультрафильтрации и электрофореза в ПААГ.
Не наблюдается прямой корреляции между повышенным уровнем оксида азота под действием Тортезина через 1 ч после инъекции и активацией метаболических процессов. Тортезин вызывает умеренное усиление гликолиза через 72 ч после введения, не вызывая достоверного изменения процессов ПОЛ.
Изучение фармакотоксикологии и общей фармакологии лекарственной формы препарата Тортезин показало, что препарат относится к классу малотоксичных соединений и не обладает кумулятивным, местно-раздражающим и аллергенным действием. Препарат нормализует общий тонус организма, продлевает и улучшает качество жизни, благотворно влияет на нервно-психический статус. Побочных эффектов препарата не обнаружено.
Проведенное клиническое исследование показало хорошую переносимость инъекции препарата Тортезин. У пациентов не отмечены жалобы или недомогания, связанные с препаратом. В первые дни после укола более 25% пациентов отмечали улучшение общего самочувствия и возрастание физической активности.
Экспериментально установлено высокое антианемическое действие Тортезина. По механизму действия Тортезин имеет несколько точек приложения, одновременно воздействуя как на иерархически высокие этажи кроветворения, т.н. «стволовые клетки», так и на процессы выброса молодых форм эритроцитов.
Препарат Тортезин относится к стресс-протекторным препаратам. Это проявляется в его влиянии на центральную нервную систему, биохимические и общесоматические показатели. В механизме стресс-протекторного действия Тортезина заметное влияние оказывает его иммуномодулирующее действие. Тортезин также оказывает ярко выраженный стабильный антидепрессивный эффект.
Перечень рекомендуемых областей применения Тортезина следует расширить, включив в него антианемическое, стресс-протекторное, антидепрессивное действие и влияние на половую функцию
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
На основании проведенных исследований разработаны нормативные документы для получения ВФС. Результаты исследования расширяют рекомендуемые области применения препарата Тортезин, что открывает перспективы коррекции некоторых гематологических и соматических заболеваний.
СПИСОК ОПУБЛИКОВАННЫХ РАБОТ
Александров В.В., Н.А.Тагайалиева, М.А.Фомина, Ю.В.Тимохина, Н.Ш.Тушакова, Назирова Э.Р., Выпова Н.Л. Влияние препарата «Тортезин» на продолжительность жизни лабораторных животных.// Фармацевтический журнал.- 2008.-№ 4.- С. 44-47.
Фомина М.А., Тушакова Н.Ш., Назирова Э.Р., Александров В.В. Влияние Тортезина на половую функцию крыс-самцов.//Материалы докладов XV Международной конференции студентов, аспирантов и молодых ученых «Ломоносов». Секция «Биология».- М.: Издательство МГУ; СП МЫСЛЬ, 2008. - С. 43.
Александров В.В., М.А.Фомина, Э.Р.Назирова, Н.Ш.Тушакова, Н.Л.Выпова. Влияние препаратов из рептилий на перекисное окисление липидов, гликолиз и углеводный обмен. // Узбекский биологический журнал.- 2010.- №1.- С. 3-6.
Пулатов Д.А., Ж.Н.Каххаров, Н.Б.Равшанова, К.А.Саидова, Н.Ш.Тушакова, Э.Р.Назирова, М.А.Фомина, В.В.Александров. Исследование клинической эффективности и переносимости Тортезина при полихимиотерапии и лучевой терапии у больных с неходжкинскими лимфомами и опухолями малого таза.//Медицинский журнал Узбекистана.- 2010.- № 2.- С. 16-19.
Александров В.В., Фомина М.А., Тушакова Н.Ш., Назирова Э.Р., Выпова Н.Л., Хасанова Г.Г., Вальтер А.Б., Тагайалиева Н.А. Влияние препаратов из рептилий на содержание некоторых типов иммуноцитов крыс.//Журнал теоретической и клинической медицины.- 2010. - № 4. - С. 11-15.
Назирова Э.Р., Александров В.В., Фомина М.А., Тушакова Н.Ш. Влияние пептидного препарата Тортезин на характер агрегации тромбоцитов.// Сборник тезисов международной научной конференции «Актуальные проблемы развития биоорганической химии». Ташкент.- 20-21 сентября 2010 г. - С.77.
Назирова Э.Р., Якубова Р.А., Александров В.В., Фомина М.А., Тушакова Н.Ш. Влияние некоторых полипептидных иммуностимуляторов на подвижность сперматозоидов человека in vitro.//Сборник научных трудов научно-практической конференции «Клиническая иммунология, иммуногенетика - междисциплинарные проблемы», с международным участием, посвященной 25-летию Института иммунологии АН РУз. Ташкент. - 11-12 октября 2010 г. - С.74-75.
Александров В.В., Тагайалиева Н.А., Фомина М.А., Тушакова Н.Ш., Назирова Э.Р. Пероральная форма препарата Тортезин из крови черепахи.// Сборник трудов Первой международной научно-практической конференции «Высокие технологии, фундаментальные и прикладные исследования в физиологии и медицине».- Санкт-Петербург, Россия.- 23-26 ноября 2010.- - СПб.: Изд-во Политехн. Ун-та, 2010. - Т.3. - С.176-180
Александров В.В., Фомина М.А., Назирова Э.Р., Тушакова Н.Ш. Расширение возможностей современных гематологических анализаторов: анализ гистограмм.//Журнал Актуальные проблемы гуманитарных и естественных наук.- Россия, Москва, 2010.- №11.- С.361-366.
Фомина М.А., Назирова Э.Р. О влиянии препарата Тортезин на содержание оксида азота.//Материалы конференции «Мустақиллик йилларида илм-фан тараққиёти: ёш олимлар муҳим фундаментал натижалари, амалий ютуқлари ва инновациялар». Сборник тезисов докладов. Ташкент.- 11 ноября 2011 г.- С.92-94.
Tagayalieva N., Dalgalarrondo M., Choiset Y., Aleksandrov V., Nazirova E., Fomina M., Tushakova N., Haertle T. Biochemical standartization of Tortezin, a novel immunostimulator from the tortoise blood cells.// Medical and Health Science Journal.- 2011. - №9. - Р.23-26.
Биология фанлари номзоди илмий даражасига талабгор Э.Р.Назированинг 03.00.04 - Биокимё ва 14.00.25 - Фармакология ихтисослиги бўйича «Тортезин препаратининг биокимёвий ва фармокологик хусусиятлари»
мавзусидаги диссертациясининг
РЕЗЮМЕСИ
Таянч сўзлар: Ўрта Осиё ташбақаси, Тортезин, қон препаратлари, биокимёвий стандартлаш, метаболик жараёнлар, фармокология, клиник тадқиқотлар, анемия, стресс.
Тадқиқот объектлари: тошбақа қонидан олинган Тортезин препаратининг дори шакли Ўз ФА Биокимё институтида экспериментал ишлаб чиқарилган.
Ишнинг мақсади: дори шаклидаги Тортезин препаратининг биокимёвий ва фармокологик хоссалари ўрганиш ва Ўзбекистон республикаси Фармакология кўмитасининг рухсат ҳужжатларини олиш учун етарли даражада тегишли тадқиқотларни ўтказиш.
Тадқиқот усуллари: флуоресцент спектроскопия, электрофорез, HPLC - хроматография, фармакологик, иммуннологик, цитологик и гематологик усуллар.
Олинган натижалар ва уларнинг янгилиги: Препаратни стандартлаштириш учун оптик, электрофоретик ва хроматографик усулларнинг имкониятлари тадқиқ қилинган. Препарат камзаҳарли бирикмалар синфига оид бўлиб, кумулятив, тушган жойини ачиштирувчи ва аллерген таъсирга эга эмас, метаболик жараёнларни ўрта даражада стимуллайди. Ўтказилган клиник тадқиқотлар препаратнинг организмда яхши ўзлашишини кўрсатди. Шунингдек, Тортезиннинг антианемик ва стресс-протекторлик ва унинг жинсий фаолияни рағбатлантирувчи таъсири аниқланди.
Амалий аҳамияти: тадқиқот натижалари препаратнинг қўлланилиш соҳаларини кенгайтиради, бу эса гематологик ва соматик хасталикларни коррекциялаш истиқболларини очиб беради.
Татбиқ этиш даражаси ва иқтисодий самарадорлиги: Ўзбекистон республикаси Фармокология қўмитасига 2010 йилда тақдим этилган материаллар асосида Тортезин препарати клиник синовларининг 2 - босқичини ўтказишга рухсат берилди (самарадорликни текшириш).
Қўлланилиш соҳаси: иммунология, гематология, онкология.
РЕЗЮМЕ
диссертации Э.Р.Назировой на тему: «Биохимические и фармакологические свойства препарата Тортезин» на соискание ученой степени кандидата биологических наук по специальностям 03.00.04 - Биохимия и 14.00.25.- Фармакология
Ключевые слова: среднеазиатская черепаха, Тортезин, препараты крови, биохимическая стандартизация препарата, метаболические процессы, фармакология, клиническое исследование, анемия, стресс.
Объект исследования: лекарственная форма препарата Тортезин из крови черепахи экспериментального производства Института биохимии АН РУз.
Цель работы: изучение биохимических и фармакологических свойств лекарственной формы препарата Тортезин и проведение соответствующих исследований в объёме, достаточном для получения разрешительных документов Фармакологического Комитета Республики Узбекистан.
Методы исследования: флуоресцентная спектроскопия, электрофорез, HPLС-хроматография, фармакологические, иммунологические, цитологические и гематологические методы.
Полученные результаты и их новизна: исследованы возможности оптических, электрофоретических и хроматографических методов для идентификации препарата. Препарат относится к классу малотоксичных соединений, не обладает кумулятивным, местно-раздражающим и аллергенным действием, вызывает умеренную стимуляцию метаболических процессов. Проведенное клиническое исследование показало хорошую переносимость препарата. Установлено антианемическое и стресс-протекторное действие Тортезина и его стимулирующее влияние на половую функцию.
Практическая значимость: результаты исследования расширяют рекомендуемые области применения препарата, что открывает перспективы коррекции некоторых гематологических и соматических заболеваний.
Степень внедрения и экономическая эффективность: на основании представленных материалов Фармкомитет РУз выдал разрешение на проведение 2-й фазы клинических испытаний препарата Тортезин (проверка эффективности).
Область применения: иммунология, гематология, онкология.
RESUME
Thesis of Nazirova Elmira Rakhimberdievna on the scientific degree competition of the candidate of science in biology on speciality: 03.00.04 - Biochemistry, 14.00.25 - Pharmacology subject: "Biochemical and pharmacological properties of Tortezin"
Key words: Central Asian tortoise, Tortezin, blood preparations, biochemical standardization, metabolic processes, pharmacology, clinical trial, anemia, stress.
Subjects of research: medical form of Tortezin preparation from the Central Asian tortoise’s blood experimentally produced by Institute of Biochemistry, Uzbekistan Academy of Sciences.
Purpose of work: to study biochemical and pharmacological properties of Tortezin’s medical form and to conduct appropriate exploration in the scope sufficient to be approved by the Uzbekistan Pharmacological Committee.
Methods of research: fluorescent spectroscopy, electrophoresis, HPLC chromatography, pharmacological, cytological and hematological methods.
The results obtained and their novelty: opportunities to identify Tortezin by means of optical, electrophoretic and chromatographic methods were studied. The preparation can be considered as the one belonging to the class of compounds with low toxicity, causing moderate stimulation of metabolic processes and possessing neither cumulative, nor locally irritating and allergic effects. Tortezin’s good tolerability by patients was demonstrated during clinical trials. Anti-anemic and stress-protective influence as well as stimulating effect of the preparation on the sexual function was established too.
Practical value: findings of the study widen recommended areas of use for the preparation opening prospects for correction of some hematological and somatic disorders.
Degree of embed and economic effectivity: given the materials submitted to the Uzbekistan Pharmacological Committee, the 2nd stage of clinical trials associated with testing of Tortezin’s efficacy was approved by the Committee.
Field of application: immunology, hematology, oncology.