Митохондриальный антиоксидант MitoQ замедляет проявление симптомов болезни Альцгеймера
Если разрезать яблоко, то через некоторое время поверхность его среза становится коричневой. Но если обрызгать яблоко выжатым лимонным соком, антиоксидантом, этот процесс замедлится. Другими словами, тот же процесс «покоричневения», известный как окислительный стресс, происходит в мозге при болезни Альцгеймера. Лежащей в ее основе причиной считается неправильный процессинг белка, связанный с образованием свободных радикалов, вызывающих окислительный стресс.
Определение молекулярных путей, ведущих к потере нервных клеток при болезни Альцгеймера, способствовало пониманию важности окислительного стресса и митохондриальной дисфункции. Митохондрии являются главным источником активных форм кислорода (АФК) и главной мишенью повреждения АФК. Чтобы защитить клетку от повреждения активными формами кислорода, в митохондриях функционируют различные антиоксидантные системы. Однако избыточная продукция АФК или нарушение антиоксидантных механизмов может привести к окислительному повреждению митохондриальных белков, липидов и ДНК.
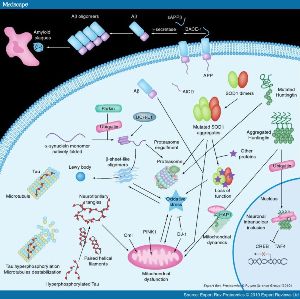
Мутации в белках, вовлеченных в развитие нейродегенеративных заболеваний, таких как болезнь Альцгеймера, ведут к их мисфолдингу и/или агрегации. Неправильно свернутые белки и их агрегаты, как правило, удаляются из клетки убиквитин-протеасомной системой, илиаутофагией. Однако перегрузка этих систем ведет к аккумуляции агрегатов в цитозоле, ядре и митохондриях. Все пути, связанные с агрегацией, сходятся на митохондриях и ведут к усилению окислительного стресса.
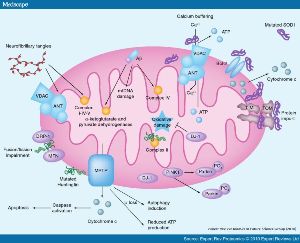
Неправильно свернутые/агрегированные и мутировавшие белки индуцируют дисфункцию Ca2+-буферизации, импорта белков, митохондриального мембранного потенциала, митохондриального дыхания и выработки АТФ, нарушение слияния/деления, повреждение митохондриальной ДНК. Конечным результатом является потеря митохондриального мембранного потенциала, приводящая, в свою очередь, к индукции митофагии и/или высвобождению из органеллы проапоптотических факторов.
Мисфолдинг и агрегация белков при нейродегенеративных заболеваниях. Мутации в белках, вовлеченных в развитие нейродегенеративных заболеваний, ведут к мисфолдингу и/или агрегации различными путями. Неправильно свернутые белки и их агрегаты удаляются из клеткиубиквитин-протеасомной системой, или аутофагией (не показана на этой схеме). Перегрузка этих систем ведет к аккумуляции агрегатов в цитозоле, ядре и митохондриях. Все пути, связанные с агрегацией, сходятся на митохондриях и ведут к усилению окислительного стресса. (Рис. medscape.com)
Ученые из Фармацевтического колледжа Университета Джорджии (University of Georgia College of Pharmacy) доказали, что антиоксидант, ориентированный непосредственно на митохондрии, может задержать проявление всех основных признаков болезни Альцгеймера, в том числе нарушения когнитивных функций. В ходе проведенного ими исследования, результаты которого опубликованы в журнале Journal of Neuroscience, генноинженерным мышам с моделью болезни Альцгеймера вводилось соединение, названноеMitoQ (mitoquinone mesylate: [10-(4,5-dimethoxy-2-methyl-3,6-dioxo-1,4-cycloheexadienl-yl) decyl triphenylphosphonium methanesulfonate]).
Адъюнкт-профессор фармацевтических и биомедицинских наук, Джеймс Фрэнклин (James Franklin), изучает процесс гибели нервных клеток, митохондриальную дисфункцию и окислительный стресс с 2004 года.
«Мозг потребляет 20 процентов кислорода организма, составляя всего 5 процентов его объема, и, таким образом, особенно чувствителен к окислительному стрессу», - объясняет доктор Фрэнклин, соавтор исследования, проведенного вместе с Меган МакМанус (Meagan McManus), PhD.
Ученые предположили, что антиоксидантов, безуспешно вводимых для лечения болезни Альцгеймера другими исследователями, недостаточно вмитохондриях клеток.
«MitoQ избирательно накапливается в митохондриях», - подчеркивает доктор МакМанус. «Для лечения более эффективно, если вещество попадает непосредственно в митохондрии, а не просто присутствует в клетке».
Митохондриальная дисфункция, индуцированная мутировавшими или неправильно свернутыми/агрегированными белками, вовлеченными в развитиенейродегенеративных заболеваний. Неправильно свернутые/агрегированные и мутировавшие белки, вовлеченные в развитие нейродегенеративных заболеваний, локализуются на митохондриальном уровне и индуцируют дисфункцию Ca2+-буферизации, импорта белков, митохондриального мембранного потенциала, митохондриального дыхания и выработки АТФ, нарушение слияния/деления, повреждение митохондриальной ДНК. Конечным результатом является потеря митохондриального мембранного потенциала, что приводит к индукции митофагии и/или высвобождению из органеллы проапоптотических факторов. (Рис. medscape.com)
Чтобы определить, в достаточной ли степени MitoQ защищает митохондрии, предотвращая тем самым развитие характерной для болезни Альцгеймера нейропатологии, in vivo , ученые использовали молодых самок генетически модифицированных мышей, несущих три гена, связанных с семейной формой болезни Альцгеймера. В течение 5 месяцев эти животные получали MitoQ с питьевой водой, а затем были протестированы на нарушение когнитивных функций с помощью лабиринта Морриса Уотера, часто используемого теста на память. Мыши, получавшие MitoQ, прошли тест значительно лучше, чем контрольные животные. Кроме того, у них не отмечалось окислительного стресса, амилоидных отложений, гибели нейронов, потери синаптических связей и активации каспаз - признаков, характерных для болезни Альцгеймера. Результаты работы позволяют говорить о центральной роли митохондрий в нейродегенерации и являются доказательствами в пользу применения при заболеваниях, сопровождающихся окислительным стрессом и метаболической недостаточностью, терапии, ориентированной на митохондрии.
По данным Общества Альцгеймера (Alzheimer's Society), в настоящее времяболезнью Альцгеймера страдают более 5 млн. американцев. Без успешной профилактики к 2050 году число больных достигнет почти 14 миллионов, и расходы на их медицинское обслуживание составят 1 триллион долларов в год.