Плоскоклеточный рак пищевода. Виды и диагностика плоскоклеточного рака пищевода.
Плоскоклеточный рак (син. эпидермоидный рак) - наиболее характерная форма рака пищевода. Мужчины болеют в 3-4 раза чаще женщин. Преобладают пациенты в возрастном интервале 50-80 лет. У лиц негроидной расы этот рак встречается в 6 раз чаще, чем у лиц европеоидной расы. В симптоматике доминируют дисфагия в отношении вначале плотной, а затем и жилкой пищи, а также прогрессирующее исхудание. Изредка к этому добавляется гиперкальцемия, развивающаяся под воздействием белка, связанного с паратиреоидным гормоном, вырабатываемым опухолевыми клетками. У 10 % больных, кроме того, может развиться метахронный, реже синхронный рак губы, языка, полости рта или небной миндалины. Выделяют две клинико-морфологические формы рака пищевода.
Поверхностный плоскоклеточный рак
Поверхностный плоскоклеточный рак (син.: ранний рак, интрамукозная карцинома) распространяется не глубже подслизистого слоя пищевода, безотносительно к тому, имеются ли метастатические поражения регионарных лимфатических узлов или нет. У больных с такой формой рака меньше выражена дисфагия, и около половины из них могут вообще не иметь симптоматики со стороны пищевода. Более 85 % пациентов с поверхностным раком пищевода выживают в течение 5 лет и более 55 % - в течение 10 лет. Изменения здесь, хотя и бывают мультицен-тричными, в сумме редко достигают протяженности в несколько сантиметров. Их внешний вид варьирует от слегка отечной зоны слизистой оболочки к эрозии с чуть приподнятыми краями, затем к бородавчатому или полиповидному возвышению или бляшковидной площадке с зернистой и эрозированной поверхностью. Под микроскопом интрамукозная карцинома характеризуется наличием небольших солидных гнезд или мелких групп раковых клеток, лежащих ниже базальной мембраны пораженного эпителия. Как правило, в этих инвазивиых очажках встречаются крупные кератиноциты, часть которых могут обладать признаками ороговения (в то время как поверхностный эпителий отличается базалоидной дифференцировкой без ороговения). Реже указанные очажки целиком подвергаются дифференцировке в базалоидном направлении.
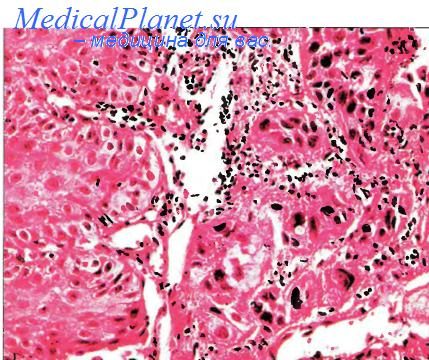
Глубоко инвазивный плоскоклеточный рак
Глубоко инвазивный плоскоклеточный рак, как правило, развивается в средней, реже нижней части грудного отдела пищевода. На верхнюю часть органа всего приходится менее 20 % наблюдений. Различают три наиболее распространенные макроскопические формы роста такого рака: грибовидную (экзофитную), язвенную (интрамуральную) и язвенно-инфильтративную (нередко стенозируюшую). Реже встречается медуллярная (трансмуральная, циркулярная) форма. Принято думать, что, начавшись в очаге(ах) карциномы in situ, раковая паренхима прорастает собственную пластинку слизистой оболочки и в течение некоторого времени существует в форме интрамукозной карциномы.
Как правило, инвазивный процесс проявляется в виде удлиненных почкующихся выростов ракового эпителия, образующих некую сеть в собственной пластинке, затем проникающих через muscularis mucosae и субмукозный слой, в котором происходят «горизонтальное распространение» и циркулярный рост опухоли. В указанном слое иногда развивается десмопластическая реакция стромы. Изредка субмукозная инвазия развивается без прорастания собственной пластинки слизистой оболочки, а прямо из очагов карциномы in situ, «ползущей» по протокам желез подслизистого слоя. В ходе инвазии у 15 % больных малигнизированные клетки пенетрируют лимфатические сосуды и венулы собственной пластинки и подслизистого слоя, приводя к формированию раковых эмболов и интрамуральных метастазов даже в адвентиииальной оболочке. У лиц с интрамуральными метастазами обычно гораздо чаще обнаруживаются метастатические поражения лимфатических узлов средостения и печени. Примерно в 23 % случаев отмечается периневральное распространение. По ходу роста раковая паренхима врастает в мышечнную оболочку пищевода и распространяется по ходу волокон, т. е. вертикально во внутреннем циркулярном слое, но горизонтально (в периферическом направлении, как в подслизистом слое) в слое plexus myentericus и внешнего продольного мышечного слоя пищевода. Достигнув адвентициальной оболочки, раковые эпителиоциты стимулируют вокруг себя десмоплазию (коллагеннизация опухолевой стромы) Инвазия за пределами пищевода обычно направлена в трахею, бронхи, кардию желудка.
Под микроскопом плоскоклеточный рак пиищевода принято разделять на три типа по степени гистологической дифференцировки (высоко-, умеренно- и низкодифференцированный), однако и здесь дифференцировка паренхимы опухолиможет сильно варьировать внутри одного и того же узла. Различия между указанными типами основываются на том или ином объеме каждого из следующих трех компонентов, представлены мелкими примитивными генерирующими клетками базального типа, крупными светлыми плоскими клетками, очагами ороговения. Чем сильнее выражен базально-клеточный компонент, тем выше митотическая активность раковой паренхимы и ниже степень гистологической дифференцировки (степень III). Такая паренхима интенсивно окрашивается моноклональным антителом AEI к низкомолекулярным цитокератинам. Чем сильнее выражены два других компонента, тем меньше склонность к митозу, выше уровень дифференцировки раковой паренхимы и слабее реакция с АЕ1 (степень I). Наиболее распространенным типом в пищеводе является умеренно-дифференцированный плоскоклеточный рак, занимающий промежуточное положение между двумя вышеописанными типами (степень II), для которого характерены нестабильные результаты реакции с АЕ1. В практической морфологической диагностике указание на ту или иную степень гистологической дифференцировки рака пищевода имеет небольшую прогностическую ценность, если у него нет признаков явной (АЕ1-негативной) анаплазии. Кроме того, нужно иметь в виду очаговые колебания уровней гистологической дифференцировки внутри одной и той же опухоли.
Примерно у 20 % больных паренхима плоскоклеточного рака пищевода включает в себя небольшие очажки железистой дифференцировки. Эти очажки могут быть представлены как отдельными клетками, продуцирующими муцины, так и группами сформированных железистых трубочек. И то, и другое обнаруживается лишь в инвазивной опухоли, но не глубже, чем в пределах собственной пластинки слизистой оболочки или поверхностных отделов подслизистого слоя. Патологи, как правило, отмечают указанные очажки в своем заключении, однако, если суммарный объем очажков приравнивается к объему эпидермо-идных структур, можно использовать традиционный термин «аденосквамозный рак».
В группе плоскоклеточного рака пищевода редко встречаются следующие разновидности: низкодифференцированный плоскоклеточный рак пищевода с обильной «лимфоцитарной стромой», напоминающий лимфоэпителиальные опухоли носоглотки, молочной железы и желудка; карцинома с базалоидными, криброзными гнездами (син. аденоид-кистозный рак), окруженными обильным гиалиновым материалом, служащим как бы добавкой к базальной мембране гнезд; псевдосаркоматозный рак (с полиповидной формой роста, а также бифазной - саркомолодобной и раковой - дифференцировкой); веррукозная карцинома с выраженным ороговением (возникающая в проксимальной трети пищевода и имеющая вид полипа или «цветной капусты»).
Плоскоклеточный рак пищевода следует дифференцировать, в первую очередь, от изменений в зоне рефлюксной (нераковой) язвы, вторичных изменений у лиц, прошедших лучевую и/или химиотерапию, а также от изъязвленного полипа.
Рак пищевода
рекомендации по диагностике, лечению и наблюдению
Заболеваемость
В среднем заболеваемость раком пищевода в Европе составляет 4,5 / 100 тыс. чел. в год при смертности 3,5 случаев на 100 тыс. чел. в год.
Диагностика
Диагноз устанавливается на основании данных эндоскопической биопсии и результатов гистологического заключения. Необходимо отдельно выделять мелкоклеточный рак от плоскоклеточного рака и аденокарциномы для проведения соответствующей терапии.
Стадирование
План обследования включает в себя клинический осмотр (включая эндоскопию верхних дыхательных и пищеварительных путей), общий и биохимический (с определением функции печени и почек) анализы, фиброэзофагогастроскопию, рентгенологическое исследование пищевода и компьютерную томографию органов грудной клетки и брюшной полости.
Бронхоскопия выполняется, если опухоль имеет связь с тархеобронхиальным деревом. Перед хирургическим лечением для оценки распространенности процесса по критериям T и N необходимо выполнение эндоскопической ультрасонографии [II, B].
При местно-распространенных (Т3/Т4) аденокарциномах пищеводно-желудочного перехода для исключения метастазирования по брюшине возможно выполнение лапароскопии [II, B].
В выборе локального метода лечения первостепенное значение имеет локализация опухоли: шейный, внутригрудной отделы или пищеводно-желудочный переход [IV, C].
Стадирование процесса осуществляется в соответствие с сиcтемой TNM и последующим определением стадии по AJCC:
|
Стадия 0 |
Tis |
No |
Mo |
|
Стадия I |
T1 |
No |
Mo |
|
Стадия IIA |
T2, T3 |
No |
Mo |
|
Стадия IIB |
T1, T2 |
N1 |
Mo |
|
Стадия III |
T3 T4 |
N1 No, N1 |
Mo Mo |
|
Стадия IVA |
Любое Т |
Любое N |
M1a* |
|
Стадия IV B |
Любое Т |
Любое N |
M1b** |
M1a*: метастазы в шейные лимфатические узлы для опухолей верхнегрудного отдела, метастазы в чревные лимфоузлы для опухолей нижнегрудного отдела. Не существует при опухолях среднегрудного отдела.M1b**: метастазы в лимфатические узлы других (нерегионарных групп) или отдаленные метастазы.
Лечение
Изначально должен рассматриваться мультидисциплинарный лечебный подход.
Операция остается стандартным лечением для операбельных пациентов с локализованными опухолями (Tis-T3 No-1 Mo). Трансторакальная эзофагэктомия с двухзональной лимфодиссекцией рекомендована при плоскоклеточном раке внутригрудной локализации [III, C]. Для опухолей шейного отдела пищевода стандартного лечения не существует. Объем хирургического лечения при аденокарциномах также все еще не определен.
Трансдиафрагмальная эзофагэктомия в сравнении с торакальным доступом с en bloc лимфаденэктомией сопровождается меньшими осложнениями. Однако выживаемость при этом может ухудшаться [I, В]. Не менее 6 регионарных лимфатических узлов должно быть иссечено и исследовано.
Пред- и послеоперационная лучевая терапия не улучшает выживаемости больных в сравнении с одной операцией [I, A]. Такое лечение не может быть рекомендовано в качестве стандартного подхода.
Интраоперационная (одна или с добавлением послеоперационной) лучевая терапия не улучшает выживаемости больных по сравнению с одной операцией. Такое лечение не может быть рекомендовано в качестве стандартного подхода.
Данных об эффективности адъювантной химио(лучевой) терапии недостаточно. Ее проведение пока не может быть рекомендовано.
Лечение ранних стадий (Tis-T1a No)
Оперативное лечение является стандартным при ранних стадиях заболеваемости. Целесообразность эндоскопической резекции слизистой оболочки еще изучается.
Лечение локализованных стадий (T1-T2N0-1)
Плоскоклеточный рак:
Операция является стандартным подходом, не смотря на то. Что при поражении регионарных лимфоузлов длительная выживаемость не превышает 25%.
При противопоказаниях к операции или отказе пациента от нее показано проведение химиолучевой терапии, эффективность которой превосходит одну лучевую [I, A].
Аденокарцинома
Операция является стандартным подходом. На выживаемость негативно влияют те же факторы, что и при плоскоклеточном раке.
Лечение местно-распространенного рака пищевода (T3-T4 N0-1)
Хирургическое лечение в качестве самостоятельного метода не является стандартным подходом при данной распространенности, поскольку радикальная резекция возможна лишь в 70% случаев при зТ3 и 50% при рТ4. Более того, длительная выживаемость после радикального хирургического лечения не превышает 15%.
Плоскоклеточный рак
Как показано в исследованиях II фазы, проведение предоперационной химиотерапии или предоперационной химиолучевой терапии повышает частоту радикальных вмешательств, уменьшает частоту местных рецидивов и, как следствие, выживаемость [II, B]. Однако существует мнение, что предоперационная химиолучевая терапия может повышать послеоперационную летальность. В недавнем рандомизированном многоцентровом французском исследовании (FFCD 9102) данная категория больных получала химиолучевое лечение с последующей операцией. Было показано, что убольных с зарегистрированным на фоне химиолучевой терапии эффектом, выполнение операции не улучшает показатели выживаемости [II, B].
Аденокарциономы
До настоящего времени неизвестно, улучшает ли лучевая терапия выживаемость в сравнении с одной предоперационной предоперационной химиотерапией, и какие пациенты будут иметь преимущество от последующего от последующего выполнения операции. Тем не менее. Совместное использование комбинации цисплатин/5-фторурацил с лучевой терапией (СОД 40Гр) и последующим хирургическим лечением может рассматриваться как один из вариантов при данных опухолях [II, B].
Лечение метастатической болезни (IV стадия)
У больных с метастатическим раком пищевода в зависимости от различных клинических ситуаций могут рассматриваться различные паллиативные решения. Стентирование пищевода является наиболее эффективным (с точки зрения стоимости) способом устранения дисфагии [III, B].
Проведение паллиативной химиотерапии возможно у отдельных пациентов [III, B].
Наблюдение
Нет данных, что регулярные наблюдения за больными после завершения начальной терапии влияют на выживаемость. Показанием к визитам должны быть симптомы. Вопросы по питанию и психосоциальные проблемы [IV, D].